Никел
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Read other articles:

Kunlun Shan beralih ke halaman ini. Untuk dermaga transportasi ampibi Tiongkok, lihat Kunlun Shan (998). Untuk tempat mitologis, lihat Gunung Kunlun (mitologi). Pegunungan Kunlun Pegunungan Kunlun adalah rangkaian pegunungan terpanjang di Asia terletak di Provinsi Qinghai di Tiongkok dan melewati perbatasan Tiongkok-India.[1][2][3] Terbentang mulai dari Pamir di Tajikistan melewati perbatasan Xinjiang dan Tibet sampai ke Provinsi Qinghai. Berjarak 1200 km, mempunyai eb...

International exposition in Kazakhstan This article is about the international exposition. For the Canadian non-profit organization, see Expo 17. This article uses bare URLs, which are uninformative and vulnerable to link rot. Please consider converting them to full citations to ensure the article remains verifiable and maintains a consistent citation style. Several templates and tools are available to assist in formatting, such as reFill (documentation) and Citation bot (documentation). (Aug...

Strada statale 546TroianaLocalizzazioneStato Italia Regioni Puglia DatiClassificazioneStrada statale InizioFoggia, innesto con la SS 90 FineTroia Lunghezza17,000[1] km Provvedimento di istituzioneD.M. 12/04/1967 - G.U. 135 del 31/05/1967[2] GestoreTratte ANAS: nessuna (dal 2001 la gestione è passata alla provincia di Foggia) Manuale La ex strada statale 546 Troiana (SS 546), ora strada provinciale 115 Foggia-Troia (SP 115)[3], è una strada provinciale itali...

Coming of Age in Samoa Judul original (1928)PengarangMargaret MeadJudul asliComing of Age in SamoaPenerjemahDatangnya Usia di SamoaNegaraAmerika SerikatBahasaBahasa InggrisSubjekKultur dan sosialitas SamoaPenerbitWilliam Morrow dan Perusahaan.Tanggal terbit1928Jenis mediaPrint)Halaman297 Coming of Age in Samoa (Bahasa Indonesia: Datangnya Usia di Samoa adalah salah satu buku dari Margaret Mead, antropolog Amerika berdasarkan penelitian dan studinya tentang pemuda - terutama rem...

Unit of the Chinese military responsible for the training of astronauts People's Liberation Army Astronaut CorpsEmblem of the People's Liberation ArmyActive1998; 26 years ago (1998)Country People's Republic of ChinaAllegiance Chinese Communist PartyBranch People's Liberation Army Strategic Support ForcePart of People's Liberation ArmyMilitary unit The People's Liberation Army Astronaut Corps (PLAAC; Chinese: 中国人民解放军航天员大队), also know...

Russian cyclist Mamyr StashStash in 2017Personal informationFull nameMamyr Basam StashBorn (1993-05-04) 4 May 1993 (age 30)Maykop, RussiaHeight1.86 m (6 ft 1 in)Weight77 kg (170 lb)Team informationCurrent teamMinsk Cycling ClubDisciplinesRoadTrackRoleRiderRider typeSprinterAmateur teams2013Russian Helicopters[1]2023–Minsk Cycling Club Professional teams2014Itera–Katusha[1]2015–2016RusVelo[1]2017–2018Lokosphinx2019Gaz...

District in Ethiopia This article relies largely or entirely on a single source. Relevant discussion may be found on the talk page. Please help improve this article by introducing citations to additional sources.Find sources: Meta Robi – news · newspapers · books · scholar · JSTOR (February 2022) Meta Robi is one of the Aanaas in the Oromia region of Ethiopia. Part of the West Shewa Zone, it is bordered on the south by Ejerie, on the southwest by Jeldu...

AS DragonsCalcio Les Monstres (I mostri) Segni distintivi Uniformi di gara Casa Trasferta Colori sociali Rosso, giallo Dati societari Città Kinshasa Nazione RD del Congo Confederazione CAF Federazione FECOFA Fondazione 1938 Stadio Cardinal-Malula(24 000 posti) Palmarès Titoli nazionali 4 Campionati della Rep. Dem. del Congo Trofei nazionali 5 Coppe della Rep. Dem. del Congo Si invita a seguire il modello di voce L'Amicale sportive Dragons, noto in passato come Amicale sportive B...

Sole heavy rail-compatible crossing of the San Francisco Bay Dumbarton Rail BridgeThe bridge in 2021.Coordinates37°29′35″N 122°06′59″W / 37.493137°N 122.116478°W / 37.493137; -122.116478Carriedsingle-track railwayCrossedSan Francisco Bay (Newark Slough)Other name(s)Dumbarton Point BridgeDumbarton BridgeNamed forDumbarton PointOwnerSamTrans[1]CharacteristicsDesignPratt through truss with central swing Pennsylvania (Petit) through truss span, tim...

Battle in Egypt in 1167 Battle of Al-BabeinPart of the CrusadesDetail of a miniature of a battle between Amaury and Siracon (Shirkuh).DateMarch 18, 1167LocationGiza, EgyptResult Zengids Victory[1][2]Belligerents Kingdom of Jerusalem Zengids of SyriaCommanders and leaders Amalric I of Jerusalem ShirkuhSaladinStrength 374 knights, some horse archers and tens of thousands(10.000+) latin crusader [3][dubious – discuss] 2,000[4][5]Casualti...

Weekly news magazine in France Le Figaro MagazineCategoriesNews magazineFrequencyWeeklyPublisherSociété du Figaro S.A.Founded1978; 46 years ago (1978)CompanyGroupe FigaroCountryFranceBased inParisLanguageFrenchWebsiteLe Figaro MagazineISSN0184-9336 Le Figaro Magazine is a French language weekly news magazine published in Paris, France. The magazine is the weekly supplement of the daily newspaper Le Figaro and has been in circulation since 1978. History This article is part...

Maslinic acid Names IUPAC name 2α,3β-Dihydroxyolean-12-en-28-oic acid Systematic IUPAC name (4aS,6aS,6bR,8aR,10R,11R,12aR,12bR,14bS)-10,11-Dihydroxy-2,2,6a,6b,9,9,12a-heptamethyl-1,3,4,5,6,6a,6b,7,8,8a,9,10,11,12,12a,12b,13,14b-octadecahydropicene-4a(2H)-carboxylic acid Other names Crategolic acid; Masilinic acid; Crataegolic acid Identifiers CAS Number 4373-41-5 Y 3D model (JSmol) Interactive image ChEBI CHEBI:66682 N ChEMBL ChEMBL201515 N ChemSpider 66312 N ECHA InfoC...
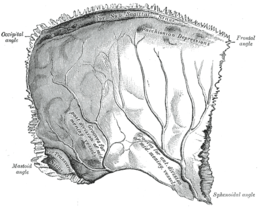
Osso parietaleOsso parietale (sinistro), superficie esternaOsso parietale (sinistro), superficie interna Anatomia del Gray(EN) Pagina 133 SistemaSistema scheletrico TipoPiatto Ossa in contattoSfenoide, frontale, temporale, occipitale ArticolazioniSutura sagittale, sutura coronale, sutura lambdoidea Inserzioni e origini muscolariTemporale IdentificatoriMeSHParietal+boneA02.835.232.781.651 TAA02.1.02.001 FMA9613 Modifica dati su Wikidata · Manuale L'osso parietale è un osso del neurocran...

Politici, ministri e alti dignitari del Manciukuò,[1] Stato fantoccio dell'Impero giapponese durante la seconda guerra mondiale Uno Stato fantoccio, a volte anche governo fantoccio, è una forma di governo che, anche se formalmente appartiene alla cultura del popolo governato, in realtà deve la sua esistenza a un'entità più potente, di solito uno Stato estero, che la controlla, l'appoggia e la difende.[2] Indice 1 Storia 1.1 Antichità 1.2 Medioevo 1.3 Il XIX secolo e i re...

2007 crime film by David Cronenberg Eastern PromisesTheatrical release posterDirected byDavid CronenbergScreenplay bySteven KnightProduced by Paul Webster Robert Lantos Starring Viggo Mortensen Naomi Watts Vincent Cassel Armin Mueller-Stahl CinematographyPeter SuschitzkyEdited byRonald SandersMusic byHoward ShoreProductioncompanies Focus Features BBC Films Astral Media Corus Entertainment Telefilm Canada Kudos Pictures Serendipity Point Films Scion Films Distributed by Pathé Distribution (Un...

The central command for all NATO maritime forces Maritime Command redirects here. For the navy of Canada, see Royal Canadian Navy. Allied Maritime CommandFounded1 December 2012TypeTactical level commandRoleCommand and control of maritime forcesPart ofAllied Command OperationsHeadquartersNorthwood Headquarters, Hertfordshire, United KingdomWebsitemc.nato.intCommandersCommanderVice Admiral Mike Utley (Royal Navy)Deputy CommanderVice Admiral Didier Maleterre (French Navy)Chief of StaffRear ...

Hospital in Selangor, MalaysiaSultan Idris Shah Serdang HospitalGeographyLocationSepang, Selangor, MalaysiaServicesEmergency departmentYesBeds763HistoryOpened2006LinksWebsiteOfficial websiteListsHospitals in Malaysia Sultan Idris Shah Serdang Hospital, previously known as the Serdang Hospital, is a government-funded multi-specialty hospital located in Sepang District, Selangor, Malaysia. The location of the hospital borders the South Klang Valley Expressway (SKVE) to the east and the Faculty...

Quartetto StarsIl Quartetto Stars nella trasmissione Rosso e nero Radio Rai 1951 Paese d'origine Italia GenereMusica leggera Periodo di attività musicale1945 – 1953 EtichettaCetra Modifica dati su Wikidata · Manuale Il Quartetto Stars era un gruppo vocale femminile torinese in attività negli anni quaranta e cinquanta. Indice 1 Storia del gruppo 2 Discografia parziale 2.1 78 giri 3 Bibliografia 4 Collegamenti esterni Storia del gruppo Il Quartetto Stars nacque...

Negara dengan kebudayaan La Tene (hijau tua) Kebudayaan La Tene adalah budaya Zaman Besi Eropa yang dinamai berdasarkan situs arkeologi La Tene di sisi utara Danau Neuchatel di Swiss, sebuah tempat yang kaya akan artefak dan ditemukan oleh Hansli Kopp pada tahun 1857.[1] Kebudayaan ini menyebar ke sebagian besar negara-negara Eropa, seperti Jerman, Prancis, Britania Raya, Irlandia, Republik Ceko, Slowakia, Slovania, Hungaria dan Rumania.[2] Ciri-cirinya tampak pada berbagai ba...

For the language, see Amarasi language. Amarasi was a traditional princedom in West Timor, in present-day Indonesia. It had an important role in the political history of Timor during the 17th and 18th century, being a client state of the Portuguese colonialists, and later subjected to the Netherlands East Indies. History Amarasi priests, father & son. The origins of Amarasi are recounted in various legends. The oldest available version says that the dynastic line originated from Wehali, t...


![{\displaystyle {\ce {3NiO + 2Al ->[{t°}] 3Ni + Al2O3}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/201526a17db13395d512a14c5f93bc0c45eaa289)