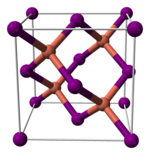
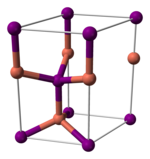
Đồng(I) iodide
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Read other articles:

SokciDaerah dengan populasi signifikan Kroasia: Slavonia dan Baranja Serbia: Vojvodina Hungaria: Kabupaten Baranya Bosnia dan Herzegovina RumaniaBahasaKroasia dan HungariaAgamaKatolik RomaKelompok etnik terkaitBunjevci, Kroasia dan Serbia Šokci (Kroasia: Šokci, Hungaria: Sokácok, Serbia: Шокци / Šokci) adalah kelompok etnis Slavia Selatan yang dianggap sebagai bagian dari etnis Kroasia. Šokci tidak dianggap sebagai identitas yang terpisah di Kroasia,[...

Liga 3 Sulawesi Selatan 2021Liga 3 Asprov PSSI Sulawesi SelatanLogo Liga 3 IndonesiaNegara IndonesiaTanggal penyelenggaraan13 November – 26 Desember 2021Tempat penyelenggaraan Lapangan M. Djunaid Hamzah, Kabupaten Sidenreng Rappang Lapangan Yonzipur 8/SMG Sakeang, Kabupaten Maros Stadion Bau Massepe, Kabupaten Pinrang Stadion FIK UNM, Kota Makassar Stadion Ganggawa, Kabupaten Sidenreng Rappang Stadion Gelora Bumi Massenrempulu Kukku, Kabupaten Enrekang Stadion Merdeka Kassi Kebo, Kabupaten ...

Artikel ini perlu diterjemahkan dari bahasa Inggris ke bahasa Indonesia. Artikel ini ditulis atau diterjemahkan secara buruk dari Wikipedia bahasa Inggris. Jika halaman ini ditujukan untuk komunitas bahasa Inggris, halaman itu harus dikontribusikan ke Wikipedia bahasa Inggris. Lihat daftar bahasa Wikipedia. Artikel yang tidak diterjemahkan dapat dihapus secara cepat sesuai kriteria A2. Jika Anda ingin memeriksa artikel ini, Anda boleh menggunakan mesin penerjemah. Namun ingat, mohon tidak men...

2021 film directed by Shakti Soundar Rajan Not to be confused with Ted (film). TeddyOfficial release posterDirected byShakti Soundar RajanWritten byShakti Soundar RajanProduced byK. E. Gnanavel RajaStarringAryaSayyeshaaSathishKarunakaranMagizh ThirumeniCinematographyS. YuvaEdited byT. ShivanandeeswaranMusic byD. ImmanProductioncompanyStudio GreenDistributed byDisney+ HotstarRelease date 12 March 2021 (2021-03-12) Running time136 minutesCountryIndiaLanguageTamil Teddy is a 2021 ...

Questa voce o sezione sull'argomento edizioni di competizioni calcistiche non cita le fonti necessarie o quelle presenti sono insufficienti. Puoi migliorare questa voce aggiungendo citazioni da fonti attendibili secondo le linee guida sull'uso delle fonti. Segui i suggerimenti del progetto di riferimento. Campionato Interregionale 1981-1982 Competizione Campionato Interregionale Sport Calcio Edizione 29ª Organizzatore Lega Nazionale Dilettanti -Comitato per l'attività Interregionale&#...

American suffragist, 1853–1945 Harriet Taylor UptonUpton, 1923Personal detailsBornHarriet Taylor(1853-12-17)December 17, 1853Ravenna, Ohio, U.S.DiedNovember 2, 1945(1945-11-02) (aged 91)Pasadena, California, U.S.Political partyRepublicanSpouseGeorge Upton (1884–1923)Signature Harriet Taylor Upton (December 17, 1853 – November 2, 1945) was an American political activist and author. Upton is best remembered as a leading Ohio state and national figure in the struggle for women's right...

2000 single by Britney Spears LuckySingle by Britney Spearsfrom the album Oops!... I Did It Again B-sideHeartReleasedJuly 25, 2000 (2000-07-25)RecordedNovember 1999StudioCheiron (Stockholm)GenreBubblegum popteen popLength3:24LabelJiveSongwriter(s) Max Martin Rami Yacoub Alexander Kronlund Producer(s) Max Martin Rami Yacoub Britney Spears singles chronology Oops!... I Did It Again (2000) Lucky (2000) Stronger (2000) Music videoLucky on YouTube Lucky is a song by American singer ...

Pour les articles homonymes, voir Alvarado. Ceylin AlvaradoInformationsNom officiel Ceylin del Carmen AlvaradoNaissance 6 août 1998 (25 ans)Cabrera (en)Nationalités dominicainenéerlandaiseÉquipes actuelles Fenix-Deceuninck (route)Alpecin-Deceuninck (cyclo-cross)Équipes UCI en cyclisme sur route 2020-3.2021Ciclismo Mundial3.2021-2022Plantur-Pura2023-Fenix-DeceuninckÉquipes cyclo-cross 2018-2019Corendon-Circus2020-6.2022Alpecin-Fenix7.2022-Alpecin-DeceuninckPrincipales victoires Cha...

Miss World 1998Tanggal26 November 1998TempatBaie Lazare, SeychellesPembawa acaraRonan Keating, Eden HarelStasiun televisiE!, SBCPeserta86Finalis/Semifinalis10DebutAngola, Kazakhstan, Sint MaartenTidak tampilCape Verde, Honduras, Latvia, Macau, Namibia, Thailand, UgandaTampil kembaliCuraçao, Liberia, Mauritius, Nicaragua, NigeriaPemenangLinor Abargil [1]( Israel)lbs Miss World 1998 adalah edisi ke-48 dari kontes kecantikan Miss World yang diadakan di Baie Lazare, S...

Prepares and publishes the United States Code Office of theLaw Revision CounselAgency overviewFormed1974JurisdictionUnited StatesAgency executiveRalph V. Seep, Law Revision CounselWebsiteuscode.house.gov The Office of the Law Revision Counsel of the United States House of Representatives prepares and publishes the United States Code, which is a consolidation and codification by subject matter of the general and permanent laws of the United States. The Office was created in 1974 when the provi...

Aida Turturro al Tribeca Film Festival 2012 Aida Turturro (New York, 25 settembre 1962) è un'attrice statunitense di origini italiane. Indice 1 Biografia 2 Premi e riconoscimenti 3 Filmografia 3.1 Cinema 3.2 Televisione 3.3 Serie TV 4 Doppiatrici italiane 5 Altri progetti 6 Collegamenti esterni Biografia Aida Turturro è conosciuta principalmente per aver interpretato la parte di Janice Soprano, sorella del boss della malavita Tony, nella pluripremiata serie televisiva HBO I Soprano, dal 200...

2016年美國總統選舉 ← 2012 2016年11月8日 2020 → 538個選舉人團席位獲勝需270票民意調查投票率55.7%[1][2] ▲ 0.8 % 获提名人 唐納·川普 希拉莉·克林頓 政党 共和黨 民主党 家鄉州 紐約州 紐約州 竞选搭档 迈克·彭斯 蒂姆·凱恩 选举人票 304[3][4][註 1] 227[5] 胜出州/省 30 + 緬-2 20 + DC 民選得票 62,984,828[6] 65,853,514[6]...

2016年美國總統選舉 ← 2012 2016年11月8日 2020 → 538個選舉人團席位獲勝需270票民意調查投票率55.7%[1][2] ▲ 0.8 % 获提名人 唐納·川普 希拉莉·克林頓 政党 共和黨 民主党 家鄉州 紐約州 紐約州 竞选搭档 迈克·彭斯 蒂姆·凱恩 选举人票 304[3][4][註 1] 227[5] 胜出州/省 30 + 緬-2 20 + DC 民選得票 62,984,828[6] 65,853,514[6]...

32°52′37″N 35°10′59″E / 32.87694444°N 35.18305556°E / 32.87694444; 35.18305556 تحتاج هذه المقالة كاملةً أو أجزاءً منها لإعادة الكتابة حسبَ أسلوب ويكيبيديا. فضلًا، ساهم بإعادة كتابتها لتتوافق معه. الدامون الإحداثيات 32°52′37″N 35°10′59″E / 32.87694444°N 35.18305556°E / 32.87694444; 35.18305556 تقسيم...

Protected wilderness area in California, United States Golden Trout WildernessIUCN category Ib (wilderness area)Lookout from the Jordan TrailMap of the United StatesShow map of CaliforniaGolden Trout Wilderness (the United States)Show map of the United StatesLocationSouthern Sierra Nevada Mountains, Tulare County / Inyo County, California, United StatesNearest cityPorterville, CaliforniaCoordinates36°18′0″N 118°19′19″W / 36.30000°N 118.32194°W / 36.300...

Copy of the cover of the Senjinkun The Instructions for the Battlefield (Kyūjitai: 戰陣訓; Shinjitai: 戦陣訓, Senjinkun, Japanese pronunciation: [se̞nʑiŋkũ͍ɴ]) was a pocket-sized military code issued to soldiers in the Imperial Japanese forces on 8 January 1941 in the name of then-War Minister Hideki Tojo.[1] It was in use at the outbreak of the Pacific War. The Senjinkun was regarded as a supplement to the Imperial Rescript to Soldiers and Sailors, which was alr...

حملة شابور الثاني العسكرية على شبه الجزيرة العربية صورة قلعة نخل وجبال الحجر. معلومات عامة التاريخ 325 الموقع سواحل الخليج العربي وشبه الجزيرة العربية النتيجة فوز ساساني حاسم انتقام العرب من الحملة بعد بضع سنوات والتسبب بخسائر بصفوف الجيش الفارسي.[1] تغييراتحدودية أنش�...

1883–1896 pair of French colonial invasions of Madagascar Franco-Hova Wars(1883–96)Part of the French colonial warsFrench poster about the Madagascar WarDateDecember 1883 – September 1895LocationMadagascarResult French victory Establishment of the Malagasy ProtectorateBelligerents France Merina KingdomCommanders and leaders Jacques Duchesne Léon Frédéric Hubert Metzinger Ranavalona III Rainilaiarivony vteScramble for Africa South Africa (1879) South Africa (1880) Tunisia (1881) Sudan...

Partai Tindakan Rakyat Nama dalam bahasa InggrisPeople's Action PartyNama dalam bahasa MelayuParti Tindakan RakyatNama dalam bahasa Mandarin人民行动党Rénmín XíngdòngdǎngNama dalam bahasa Tamilமக்கள் செயல் கட்சிMakkaḷ Ceyal KaṭciSingkatanPAPKetua umumGan Kim YongSekretaris JenderalLee Hsien LoongWakil KetuaMasagos ZulkifliAsisten Sekretaris JenderalHeng Swee KeatChan Chun SingPendiriLee Kuan YewLim Chin SiongS. RajaratnamToh Chin ChyeLim Kim SanDib...

Coordenadas: 43° 30' N 5° 5' E Bocas do RódanoBouches-du-Rhône Informações País França Região Provença-Alpes-Costa Azul Sede do depto. (Préfecture) Marselha Sub-sedes (Sous-préfectures) Aix-en-ProvenceArlesIstres População 1 975 896 hab. (2011) Área 5 087 km² Densidade populacional 388,4 hab./km² Arrondissements 4 Cantões 57 Comunas 119 Presidente do conselho geral Jean-Noël Guérini Site Oficial www.bouches-du-rhone.pref.gouv.fr Localização L...