Vanadi(III) iodide
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Read other articles:

Invasi Persia kedua ke YunaniBagian dari Perang Yunani-PersiaPeta invasi Persia kedua ke YunaniTanggal480 SM–479 SMLokasiThrakia, Thessalia, Boiotia, Attika, IoniaHasil Kemenangan Yunani hilangnya ancaman Persia dari Yunani daratan; pembebasan Kepulauan AegeaPihak terlibat Negara kota Yunani, dipimpin oleh Athena dan Sparta Kekasiaran PersiaTokoh dan pemimpin Themistokles,Eurybiades,Leonidas I†,PausaniasLeotykhides Xerxes I, Mardonios† Hydarnes lbsPerang Yunani-Persia Pemberontakan Ioni...

Pour les articles homonymes, voir JCI. Jeune Chambre Economique Française Cadre But Créer des changements positifs pour construire une paix universelle, globale et définitive[1] Zone d’influence France Fondation Fondation 1952 Fondateur Yvon Chotard Identité Siège 9/11, rue Alasseur, 75015, Paris, France Président Thomas Guest Vice-président Hélène Saintobert Secrétaire général Mathilde Quintard Trésorier Pauline Le Galloudec Affiliation européenne JCI Europe Affiliation inte...

العلاقات الأردنية المنغولية الأردن منغوليا الأردن منغوليا تعديل مصدري - تعديل العلاقات الأردنية المنغولية هي العلاقات الثنائية التي تجمع بين الأردن ومنغوليا.[1][2][3][4][5] مقارنة بين البلدين هذه مقارنة عامة ومرجعية للدولتين: وجه المقارن...

le Bel Rio Caractéristiques Longueur 18,66 km [1] Bassin collecteur Loire Organisme gestionnaire SMABCAC Régime Pluvial Cours Source Les Grands-Chézeaux · Localisation Les Grands-Chézeaux · Altitude 300 m · Coordonnées 46° 21′ 11″ N, 1° 24′ 27″ E Confluence l'Anglin · Localisation Chaillac · Altitude 134 m · Coordonnées 46° 26′ 09″ N, 1° 18′ 29″ E Géographie Principaux affluents · Riv...

Artikel atau bagian mungkin perlu ditulis ulang agar sesuai dengan standar kualitas Wikipedia. Anda dapat membantu memperbaikinya. Halaman pembicaraan dari artikel ini mungkin berisi beberapa saran.Artikel ini menggunakan kata-kata yang berlebihan dan hiperbolis tanpa memberikan informasi yang jelas. Silakan buang istilah-istilah yang hiperbolis tersebut. (Pelajari cara dan kapan saatnya untuk menghapus pesan templat ini) Spring Framework adalah salah satu jenis kerangka kerja yang bersifat o...

Valentina Domenici, chimiste italienne, analysant de l'huile d'olive La chimie alimentaire est la branche de la chimie qui étudie la composition des aliments et leur évolution au cours de la fabrication, du stockage, de la préparation et de la digestion. Elle s'intéresse aux réactions chimiques impliquant les substances présentes dans les aliments. Les réactions améliorant la conservation et certaines propriétés (organoleptiques, nutritives, etc.) du produit sont recherchées. ...
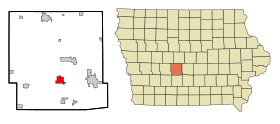
أدل الإحداثيات 41°37′00″N 94°01′18″W / 41.616666666667°N 94.021666666667°W / 41.616666666667; -94.021666666667 [1] تاريخ التأسيس 1847 تقسيم إداري البلد الولايات المتحدة[2][3] التقسيم الأعلى مقاطعة دالاس عاصمة لـ مقاطعة دالاس خصائص جغرافية المساحة 12.174736 كيل...

Dieser Artikel befasst sich mit der Haushaltsgerätemarke Foron; zu weiteren gleichnamigen Bedeutungen siehe Foron (Begriffsklärung). Typenschild und Bedienpanel einer Foron-Waschmaschine Foron war der Markenname eines Herstellers von Haushaltsgeräten („Weiße Ware“) in der Deutschen Demokratischen Republik und dem wiedervereinigten Deutschland. Inhaltsverzeichnis 1 Geschichte 2 Produkte 3 Ausstellung 4 Weblinks 5 Einzelnachweise Geschichte Deutsche Kühl- und Kraftmaschinen GmbH Schar...

Negara Plurinasional Bolivia Artikel ini adalah bagian dari seri Politik dan KetatanegaraanBolivia Konstitusi Sejarah Hak Asasi Manusia Eksekutif Presiden (daftar) Luis Arce Wakil Presiden David Choquehuanca Kabinet Bolivia Legislatif Majelis Legislatif Plurinasional Kamar Senator Presiden Senat Deputi Presiden Dewan Perwakilan Rakyat Pengadilan Mahkamah Agung Mahkamah Konstitusi Mahkamah Agung (1825–2012) Pemilu Organ Pemilihan Plurinasional Partai politik Pemilihan baru-baru ini 2020 (umu...

انقلاب 1980 في غينيا بيساو التاريخ 14 نوفمبر 1980 البلد غينيا بيساو الموقع بيساو 11°51′00″N 15°34′00″W / 11.85°N 15.566666666667°W / 11.85; -15.566666666667 تعديل مصدري - تعديل في 14 نوفمبر 1980، وقع انقلاب غبر دموي في غينيا بيساو، بقيادة رئيس الوزراء الجنرال جواو برناردو ف�...

本條目存在以下問題,請協助改善本條目或在討論頁針對議題發表看法。 此條目需要編修,以確保文法、用詞、语气、格式、標點等使用恰当。 (2013年8月6日)請按照校對指引,幫助编辑這個條目。(幫助、討論) 此條目剧情、虛構用語或人物介紹过长过细,需清理无关故事主轴的细节、用語和角色介紹。 (2020年10月6日)劇情、用語和人物介紹都只是用於了解故事主軸,輔助�...

American actor Steve BarclayBarclay in the 1953 film Noi peccatoriBorn(1918-11-20)20 November 1918Baltimore, Maryland, U.S.Died2 February 1994(1994-02-02) (aged 75)Rome, Lazio, ItalyOccupation(s)Actor, producerYears active1943–1964 (film) Stephen Barclay (20 November 1918, in Baltimore – 2 February 1994, in Rome) was an American film actor known for his work in Italy.[1][2] He became a leading man in Italian films after working in numerous Westerns in Hollywood.&...

2014 UK local government election Map of the results of the 2014 Carlisle City Council election. Labour in red, Conservatives in blue and independent in light grey. Wards in dark grey were not contested in 2014. The 2014 Carlisle City Council election took place on 22 May 2014 to elect members of Carlisle District Council in Cumbria, England. One third of the council was up for election and the Labour Party stayed in overall control of the council.[1] After the election, the compositi...

دائرة مصطفى بن إبراهيم دائرة مصطفى بن إبراهيم الإدارة ولاية سيدي بلعباس مركز الدائرة مصطفى بن إبراهيم البلديات التابعة 4 بعض الأرقام المساحة الإجمالية النسبة من مساحة الولاية السكان 31462 (احصاء: 2008[1] ) كثافة تعديل مصدري - تعديل دائرة مصطفى بن إبراهيم دائرة إدارية في �...

Aspect of English history This article is about the English city. For the U.S. city, see Timeline of Worcester, Massachusetts and Worcester, Massachusetts § History. View of Worcester looking south along River Severn (1750)Worcester's early importance is partly due to its position on trade routes, but also because it was a centre of Church learning and wealth, due to the very large possessions of the See and Priory accumulated in the Anglo-Saxon period. After the reformation, Worcester ...

Battle between Japanese and Allied forces in 1944 Battle of Imphal (Meitei: Japan Laan[1][2])Part of the Operation U-Go during the Burma Campaign in the South-East Asian theatre of World War IIGurkhas advancing with Grant tanks to clear the Japanese from Imphal-Kohima road in North Eastern British IndiaDate8 March – 3 July 1944LocationImphal, Manipur Kingdom, India24°49′00″N 93°57′00″E / 24.8167°N 93.9500°E / 24.8167; 93.9500Result British...

Nigerian professional wrestler (born 1994) This article is about the professional wrestler. For other uses, see Omo. OmosOmos in 2023Birth nameTolulope OmogbehinBorn (1994-05-16) May 16, 1994 (age 30)Lagos, Nigeria[1]Spouse(s) Cheyenne Quailey (m. 2023)Professional wrestling careerRing name(s)Jordan Omogbehin Omos[2]Billed height7 ft 3 in (221 cm)[2]Billed weight416 lb (189 kg)[2]Trained byWWE Perform...

Prima Divisione 1933Dettagli della competizioneSport Pallacanestro Edizione3ª OrganizzatoreFIP Federazione FIP Periodo19 mar —23 lug 1933 Data1933 Squadre23 (in 8 gironi) VerdettiCampioneS.G.M Forza e Coraggio 1870(2º titolo) PromozioniU.S. Bari Cronologia della competizioneed. successiva → ← ed. precedente Modifica dati su Wikidata · Manuale La Prima Divisione 1933 ha rappresentato il secondo livello del 13º campionato italiano di pallacan...

باول غرينير معلومات شخصية الميلاد 29 يناير 1768 زارلوييس الوفاة 18 أبريل 1827 (59 سنة) مواطنة فرنسا مناصب عضو الجمعية الوطنية الفرنسية في المنصب20 أكتوبر 1818 – 16 يناير 1821 الحياة العملية المهنة سياسي، وضابط، وعسكري اللغات الفرنسية الخدمة ال...

Ancient Greek vase painter The AffecterWarrior's departure, neck-amphora by the Affecter, dated 540–530 BCE, located in the Louvre MuseumBornUnknown. Named for the affected style.Before 540 BCEDiedAbout or after 520 BCENationalityGreekKnown forPottery manufacture, vase paintingNotable work135 vases, mainly amphorae, manufactured in AthensMovementBlack-figure stylePatron(s)Mainly the Etruscan market Dionysos and Ikarios on an amphora found at Vulci, British Museum (GR 1836.2–24.46) Th...