Оксид хлора(I) |
Read other articles:

This article is an orphan, as no other articles link to it. Please introduce links to this page from related articles; try the Find link tool for suggestions. (September 2023) Bahdinan prisoners is used to refer to the arrest of a group of four journalists and an activist in the Bahdinan area of Kurdistan Region. The term only became used when the group were convicted of spying[1] by the KDP on 16 February 2021. The term was used by the speaker of parliament Rewaz Faeq to refer to the...

Artur Nikolayevich ChilingarovArtur Nikolayevich Chilingarov mengunjungi Arkangelsk (22 Agustus 2009)Lahir25 September 1939 (umur 84)Leningrad, SFSR Rusia, Uni Soviet (sekarang St. Petersburg, Rusia)KebangsaanRusiaTahun aktif1963–sekarangDikenal atasPenjelajahan kutubPenghargaanPahlawan Uni SovietPahlawan RusiaOrdo LeninTanda tangan Artur Nikolayevich Chilingarov (Rusia: Артур Николаевич Чилингаровcode: ru is deprecated ; lahir 25 September 1939) adalah s...
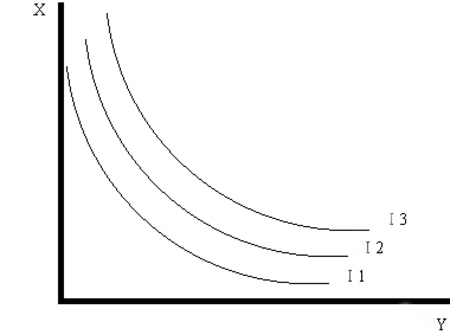
هذه المقالة بحاجة لصندوق معلومات. فضلًا ساعد في تحسين هذه المقالة بإضافة صندوق معلومات مخصص إليها. نظرية المستهلك، هي نظرية في علم الاقتصاد وتهدف إلى خلق معادلة لوصف تصرف عدّة متغيرات اقتصادية مثل المستهلك والسلعة أو الخدمة وكذلك الاشراف على الطلب، ومن خلال النظرية نرى ان...

Ancient Indian religious tradition For other uses, see Bhagavata (disambiguation). BhagavataHistorically, the Bhagavatas worshipped Vāsudeva-Krishna.[1][2] An early depiction of Vāsudeva-Krishna on a coin of Agathocles of Bactria, 190–180 BCE.[3][4] Part of a series onVaishnavism Supreme deity Vishnu / Krishna / Rama Important deities Dashavatara Matsya Kurma Varaha Narasimha Vamana Parasurama Rama Balarama Krishna Buddha Kalki Other forms Dhanvantari Guruv...

George William de Saulles (4 February 1862 – 21 July 1903) was a British medallist. He designed the obverse of coins of the United Kingdom and its colonies under Queen Victoria and King Edward VII. Life He was born on 4 February 1862 at Villa Street, Aston Manor, Birmingham. His grandfather Samuel was from Switzerland and had been a Page of the Presence in the household of George IV and William IV; his father, William Henry de Saulles, was a Birmingham glass merchant. At an early age he be...

Fibrocartilaginous part of a bone joint For other uses, see Meniscus (disambiguation). MeniscusHead of right tibia seen from above, showing menisci and attachments of ligamentsLeft knee-joint from behind, showing interior ligamentsDetailsIdentifiersLatinmeniscusGreekμηνίσκος (meniskos)MeSHD000072600TA98A03.0.00.033TA21544Anatomical terminology[edit on Wikidata] A meniscus (pl.: menisci or meniscuses) is a crescent-shaped fibrocartilaginous anatomical structure that, in contrast to...

Державний комітет телебачення і радіомовлення України (Держкомтелерадіо) Приміщення комітетуЗагальна інформаціяКраїна УкраїнаДата створення 2003Керівне відомство Кабінет Міністрів УкраїниРічний бюджет 1 964 898 500 ₴[1]Голова Олег НаливайкоПідвідомчі ор...
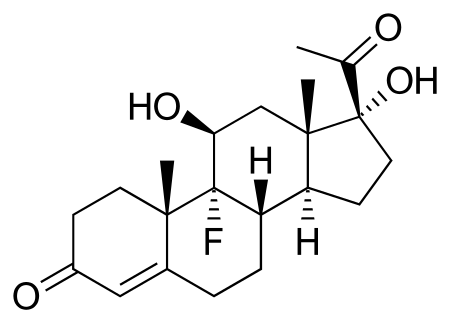
Chemical compound FlugestoneIdentifiers IUPAC name (8S,9R,10S,11S,13S,14S,17R)-17-acetyl-9-fluoro-11,17-dihydroxy-10,13-dimethyl-1,2,6,7,8,11,12,14,15,16-decahydrocyclopenta[a]phenanthren-3-one CAS Number337-03-1PubChem CID254765ChemSpider223326UNIINT3ET34748KEGGD07968CompTox Dashboard (EPA)DTXSID0048765 ECHA InfoCard100.005.830 Chemical and physical dataFormulaC21H29FO4Molar mass364.457 g·mol−13D model (JSmol)Interactive image SMILES CC(=O)C1(CCC2C1(CC(C3(C2CCC4=CC(=O)CCC43C)F)O)C)O ...

جيانكارلو مالدونادو معلومات شخصية الاسم الكامل جيانكارلو جورجيو مالدونادو ماريرو الميلاد 29 يونيو 1982 (العمر 41 سنة)كاراكاس الطول 1.73 م (5 قدم 8 بوصة) مركز اللعب مهاجم الجنسية فنزويلا فنزويلا سان كريستوبال الأب كارلوس فابيان مالدونادو معلومات النادي النادي ا...

LG ChemSebelumnya Lak Hui Chemical (1947-1966) Lak Hui Chemical Industries (1966-1973) Lucky Ltd. (1973-1995) JenisPublikKode emitenKRX: 051910, KRX: 051915IndustriBahan kimiaDidirikan1947 (didaftarkan kembali sebagai badan hukum pada tahun 2001)KantorpusatSeoul, Korea SelatanProdukBahan mentah, bahan kimia, bahan elektronik dan teknologi informasi, solusi energiPendapatan US$ 20,4 milyar (2012)[1]Laba bersih US$ 1,9 milyar (2010)[1]Karyawan20.000+ (2015)IndukLG CorporationSit...

Pour les articles homonymes, voir capitale de la culture. Capitale italienne de la culture Capitale italiana della cultura Bergame et Brescia capitales italiennes de la culture en 2023 Lieu 2023 : Bergame et Brescia Période Annuelle Date de création 2015 Structure-mère Ministère de la Culture (Ministero della cultura) Tutelle Italie Site web www.capitalicultura.beniculturali.it modifier Le titre de Capitale italienne de la culture est un label attribué pour une année entièr...

Aviation magazine FlyingJune 2016 coverCategoriesAviation magazineFrequencyMonthlyPublisherLisa DeFrees[1]Total circulation(December 2012)200,737[2]Founded1927CompanyFlying Media Group[3]CountryUnited StatesBased inWinter Park, FloridaLanguageEnglishWebsitewww.flyingmag.comISSN0015-4806 Flying, sometimes styled FLYING, is an aviation magazine published since 1927 and called Popular Aviation prior to 1942, as well as Aeronautics for a brief period. It is read by pilots,...

この項目では、兵庫県を流れる河川について説明しています。流域に位置する同名の自治体については「加古川市」をご覧ください。 加古川 大門橋下の瀬水系 一級水系 加古川種別 一級河川延長 96 km平均流量 29 m³/s(国包観測所 2002年)流域面積 1,730 km²水源 粟鹿山(兵庫県)水源の標高 962 m河口・合流先 播磨灘(兵庫県)流域 日本兵庫県・大阪府 テンプレー�...

Language family of northern Australia JarrakanDjeraganGeographicdistributionfrom Halls Creek to Wyndham and Kununurra along the Ord River in the eastern Kimberley regionLinguistic classificationOne of the world's primary language familiesSubdivisions Kija Miriwoongic Glottologjarr1235Jarrakan languages (purple), among other non-Pama-Nyungan languages (grey) The Jarrakan (formerly Djeragan) languages are a small family of Australian Aboriginal languages spoken in northern Australia. The name i...

Seaside village in County Donegal, Ireland Village in Ulster, IrelandNarin An FhearthainnVillageNarin strandNarinLocation in IrelandCoordinates: 54°50′19″N 8°26′47″W / 54.838748°N 8.446482°W / 54.838748; -8.446482CountryIrelandProvinceUlsterCountyCounty DonegalTime zoneUTC+0 (WET) • Summer (DST)UTC-1 (IST (WEST))Irish Grid ReferenceG818944 Narin (Irish: An Fhearthainn),[1] also Naran, is a small seaside village and townland in the parish...

Confederate States Army general and Ku Klux Klan leader (1821–1877) This article is about the Confederate general. For other uses, see Nathan Bedford Forrest (disambiguation). Nathan Bedford ForrestBirth nameNathan Bedford ForrestNickname(s)Old Bed[1]Wizard of the Saddle[2]Born(1821-07-13)July 13, 1821Chapel Hill, Tennessee, U.S.DiedOctober 29, 1877(1877-10-29) (aged 56)Memphis, Tennessee, U.S.BuriedColumbia, Tennessee, U.S.Allegiance Confederate StatesService/bran...

此條目介紹的是1920年—1991年存在的澳大利亚共产党。关于1971年成立时取名为“澳大利亚社会党”、1996年改名为“澳大利亚共产党”的政党,请见「澳大利亚共产党 (1996年)」。 澳大利亚共产党(1920—1944年;1951年—1991年)澳大利亚的共产党(1944年—1951年)简称CPA、ACP创始人乔克·加登(英语:Jock Garden)汤姆·沃尔什(英语:Tom Walsh (trade unionist))威廉·伊尔斯曼(...

列支敦士登的卫星图像。 瓦杜茲市中心北面景观。 列支敦斯登是欧洲西部的一個的內陸國家,與烏茲別克並列為世界上僅有的兩個雙重內陸國。 列支敦斯登坐落於歐洲阿爾卑斯山地的萊因河谷,其西邊是以萊因河作為邊界與瑞士相鄰,東側則是以屬於阿爾卑斯山脈的山嶺地帶與奧地利為界。全國只有西側約三分之一的面積位在平坦的河谷裡,其餘地區大都屬於山地。 列支�...

Questa voce sull'argomento centri abitati della California è solo un abbozzo. Contribuisci a migliorarla secondo le convenzioni di Wikipedia. Segui i suggerimenti del progetto di riferimento. Fort WashingtonCDP(EN) Fort Washington, California LocalizzazioneStato Stati Uniti Stato federato California ConteaFresno TerritorioCoordinate36°52′45.12″N 119°45′39.6″W36°52′45.12″N, 119°45′39.6″W (Fort Washington) Altitudine112 m s.l.m. Superficie0,321 k...

Sohn Won-yil-class submarine ROKS An Jung-geun on 4 June 2008 History South Korea Name An Jung-geun (안중근) NamesakeAn Jung-geun BuilderHyundai Laid down2005 Launched4 June 2008 Acquired30 November 2009 Commissioned1 December 2009 IdentificationPennant number: SS-075 StatusActive General characteristics Class and typeSohn Won-yil-class submarine Displacement 1,690 t (1,660 long tons) (surfaced) 1,860 t (1,830 long tons) (submerged) Length65 m (213 ft 3 in) Beam6.3...








