Eszopiclona
|
Read other articles:

Benetton B195KategoriFormula OneKonstruktorBenetton Formula Ltd.PerancangRoss BrawnRory ByrnePendahuluB194PenerusB196Spesifikasi teknis[1]SasisCarbon fibre monocoqueSuspensi (depan)Double wishbone, pushrodSuspensi (belakang)Double wishbone, pushrodMesinRenault RS7, 3.000 cc (183,1 cu in), 67° V10, NA, mid-engine, longitudinally mountedTransmisiBenetton transverse 6-speed semi-automaticBahan bakarElfBanGoodyearSejarah kompetisiTim pemakaiMild Seven Benetton RenaultPemba...

Emanuel Kara Penjabat Bupati Flores Timur ke-5Masa jabatan26 Juli 2016 – 22 Mei 2017PresidenJoko WidodoGubernurFrans Lebu Raya PendahuluYosep Lagadoni HerinPenggantiAntonius Hubertus Gege Hadjon Informasi pribadiLahir(1958-12-31)31 Desember 1958Keluwain, Flores Timur, Nusa Tenggara TimurMeninggal8 Oktober 2020(2020-10-08) (umur 61)RSUD Prof. Dr. W. Z. Johannes Kupang, Nusa Tenggara TimurSuami/istriIr. Agnes Palang BolenAnak2Alma materUniversitas Nusa CendanaProfesiBirokrat...

Artikel ini perlu dikembangkan dari artikel terkait di Wikipedia bahasa Inggris. (Maret 2023) klik [tampil] untuk melihat petunjuk sebelum menerjemahkan. Lihat versi terjemahan mesin dari artikel bahasa Inggris. Terjemahan mesin Google adalah titik awal yang berguna untuk terjemahan, tapi penerjemah harus merevisi kesalahan yang diperlukan dan meyakinkan bahwa hasil terjemahan tersebut akurat, bukan hanya salin-tempel teks hasil terjemahan mesin ke dalam Wikipedia bahasa Indonesia. Janga...

Strada statale 125 var Orientale SardaLocalizzazioneStato Italia Regioni Sardegna Province CagliariSud Sardegna Nuoro DatiClassificazioneStrada statale InizioSS 554 bis presso Capitana FineSS 125 presso Tortolì Lunghezza84,185[1] km Data apertura2002[2] GestoreTratte ANAS: divisa in due tronconi: dal km 0 (Capitana) al km 64,530 (Cantoniera San Giorgio) e dal km 82,765 (Tertenia) al km 108,420 (Tortolì) Manuale La strada statale 125 var Orientale Sarda (S...

Ini adalah nama Batak Toba, marganya adalah Hutapea. Hotman Paris HutapeaLahir20 Oktober 1959 (umur 64)Laguboti, Toba, Sumatera Utara, IndonesiaAlmamaterUniversitas Katolik ParahyanganUniversitas Teknologi SydneyUniversitas Gadjah MadaUniversitas PadjadjaranPekerjaanPengacarapewarapebisnisSuami/istriAgustianne Marbun, S.H., M.Hum. (m. 1989)Anak3 Dr. Hotman Paris Hutapea, S.H., LL.M., M.Hum. (lahir 20 Oktober 1959), adalah pengacara, pewara, dan pebi...

Questa voce sull'argomento stagioni delle società calcistiche italiane è solo un abbozzo. Contribuisci a migliorarla secondo le convenzioni di Wikipedia. Segui i suggerimenti del progetto di riferimento. Voce principale: Unione Sportiva Vibonese Calcio. Unione Sportiva Vibonese CalcioStagione 2011-2012Sport calcio Squadra Vibonese Allenatore Elio Ferrante e Franco Viola poi Alfonso Ammirata Presidente Giovanni Caffo Lega Pro Seconda Divisione17º posto nel girone B. Retrocede in ...

Cet article possède des paronymes, voir Les Tontons tringleurs et Les Tontons farceurs. Les Tontons flingueurs Affiche secondaire du film, montrant les mots d'argot utilisés et leur signification. Données clés Réalisation Georges Lautner Scénario Albert SimoninGeorges Lautner (non crédité) Acteurs principaux Lino VenturaBernard BlierJean LefebvreFrancis BlancheVenantino VenantiniRobert DalbanSabine SinjenClaude Rich Sociétés de production GaumontLes Films CoronaUltra FilmSicilia Ci...

Сельское поселение России (МО 2-го уровня)Новотитаровское сельское поселение Флаг[d] Герб 45°14′09″ с. ш. 38°58′16″ в. д.HGЯO Страна Россия Субъект РФ Краснодарский край Район Динской Включает 4 населённых пункта Адм. центр Новотитаровская Глава сельского пос�...

Type of modified car 2016 champion Jordan Grabouski 2006 IMCA Modified national champion Benji LaCrosse IMCA Modified is the top modified division sanctioned by the International Motor Contest Association.[1] The series began in 1979. It was designed to be a mid-level class between late models and hobby stocks.[2] The first IMCA modified race was held at the Benton County, Iowa Speedway in 1979 on a 1/4 mile track.[3] The car bodies are hybrids of open wheel cars and s...

ヨハネス12世 第130代 ローマ教皇 教皇就任 955年12月16日教皇離任 964年5月14日先代 アガペトゥス2世次代 レオ8世個人情報出生 937年スポレート公国(中部イタリア)スポレート死去 964年5月14日 教皇領、ローマ原国籍 スポレート公国親 父アルベリーコ2世(スポレート公)、母アルダその他のヨハネステンプレートを表示 ヨハネス12世(Ioannes XII、937年 - 964年5月14日)は、ロ...

The ReVe Festival: FinaleSampul digital dan versi FinaleAlbum kompilasi karya Red VelvetDirilis23 Desember 2019 (2019-12-23)Direkam2019StudioSM Studio, Seoul, Korea SelatanGenrePopR&Bpop elektrohousefuture basstrapdoo-wopfunkDurasi55:35BahasaKoreaLabelSMDreamusProduserLee Soo-man (eksekutif)KenzieAndrew ScottCazzi OpeiaEJAEDruskiYoo Young-jinMoonshineLouise Frick SveenRoyal DiveAndreas ÖbergSimon PetrénMaja KeucHwang Chan-heeHong So-jinKronologi Red Velvet The ReVe Festival: Da...
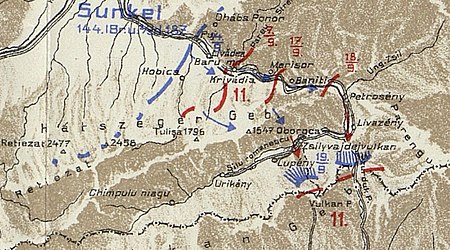
For other battles at the same location, see Second Battle of Petrozsény and Third Battle of Petrozsény. First Battle of PetrozsényPart of the Battle of Transylvania of the Romanian Campaign of World War ICourse of the battle from 17 to 19 SeptemberDate17 – 22 September 1916LocationPetrozsény and the surrounding area, Transylvania, Austria-Hungary (today Petroșani, Romania)Result German victoryBelligerents Romania German EmpireCommanders and leaders Ioan Culcer Ioan Muică&#...

Munisipalitas Cerkno Občina CerknoMunisipalitasNegara SloveniaIbu kotaCerknoLuas • Total131,6 km2 (508 sq mi)Populasi (2013) • Total4.786 • Kepadatan3,6/km2 (9,4/sq mi)Kode ISO 3166-2SI-014 Munisipalitas Cerkno (dibaca [ˈtseːɾknɔ]; bahasa Slovenia: Občina Cerkno) adalah sebuah munisipalitas di kawasan Littoral, Slovenia.[1] Kursi munisipalitas tersebut adalah kota Cerkno. Munisipalitas tersebut memiliki 5...

Overview of the use of capital punishment in Armenia Flag of Armenia Capital punishment in Armenia was a method of punishment that was implemented within Armenia's Criminal Code and Constitution until its eventual relinquishment in the 2003 modifications made to the Constitution.[1] Capital punishment's origin in Armenia is unknown, yet it remained present in the Armenia Criminal Code of 1961, which was enforced and applied until 1999.[2] Capital punishment was incorporated in...

American mobster Waxey GordonGordon's 1933 mugshotBornIrving WexlerJanuary 19, 1888Lower East Side, New York City, U.S.DiedJune 24, 1952(1952-06-24) (aged 64)Alcatraz Federal Penitentiary, San Francisco, California, U.S.NationalityAmericanOccupation(s)Bootlegger, racketeerConviction(s)Tax evasion, Narcotics traffickingCriminal penalty10 years, 25 years Waxey Gordon (born Irving Wexler; January 19, 1888 – June 24, 1952) was an American gangster who specialized in bootlegging and ill...

1913–2000 American comic strip Jiggs and Maggie redirects here. For the film series, see Jiggs and Maggie (film series). Bringing Up FatherBringing Up Father (January 31, 1920)Author(s)George McManusCurrent status/scheduleConcludedLaunch dateJanuary 2, 1913 (January 2, 1913)End dateMay 28, 2000 (2000-05-28)Alternate name(s)Maggie & Jiggs Syndicate(s)King Features SyndicateGenre(s)Humor Bringing Up Father is an American comic strip created by cartoonist George McManus...

مديرية العبر - مديرية - تقسيم إداري البلد اليمن[1] الإقليم الفدرالي إقليم حضرموت المحافظة محافظة حضرموت خصائص جغرافية إحداثيات 16°05′00″N 47°30′00″E / 16.08333°N 47.5°E / 16.08333; 47.5 المساحة 7460.90 كم² الارتفاع 812 متر السكان الكثافة السكانية 0.448 نسمة/كم2 ال�...

جواز سفر كوبيمعلومات عامةنوع المستند جواز سفرالغرض التعريف (هوية شخصية)صادر عن كوباصالح في كوبامتطلبات الاستحقاق الجنسية الكوبيةتعديل - تعديل مصدري - تعديل ويكي بيانات تصدر جوازات سفر الكوبية لمواطني كوبا لتسهيل السفر الدولي. وهي صالحة لمدة 6 سنوات من تاريخ صدورها، ولك...

Leixões Sport ClubCalcio Os Bébés, Heróis do Mar Segni distintiviUniformi di gara Casa Trasferta Terza divisa Colori sociali Rosso, bianco Dati societariCittàMatosinhos Nazione Portogallo ConfederazioneUEFA Federazione FPF CampionatoSegunda Liga Fondazione1907 Presidente Jorge Moreira Allenatore Carlos Fangueiro StadioEstádio do Mar(8.100 posti) Sito webleixoessc.pt Palmarès Trofei nazionali1 Coppe di Portogallo Si invita a seguire il modello di voce Il Leixões Sport Club, o semp...

提示:此条目页的主题不是中華民國—阿爾及利亞關係。 關於其他「中」字國家與「阿」字國家的外交關係,詳見中阿關係 (消歧義)。 中國—阿爾及利亞關係 阿尔及利亚 中國 代表機構阿爾及利亞駐華大使館中國駐阿爾及利亞大使館代表大使 拉赫桑·卡伊德·苏莱曼[1]大使 李健 中國—阿尔及利亚关系(阿拉伯语:العلاقات الصينية الجزائر�...


