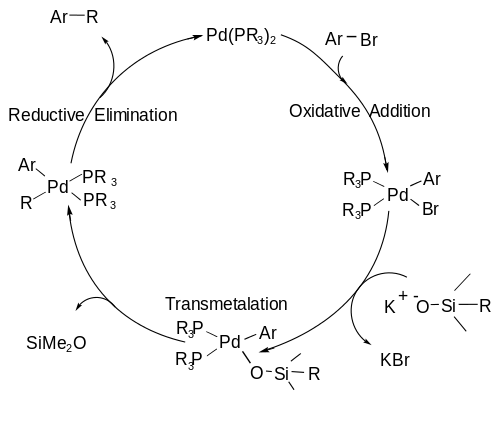
Reazione di accoppiamento di Hiyama
|
Read other articles:

Not to be confused with Coffee percolator. Device used for brewing coffee Moka potManufacturerBialettiRelease date1933 The moka pot[1][2] is a stove-top or electric coffee maker that brews coffee by passing hot water driven by vapor pressure through ground coffee. Named after the Yemeni city of Mocha, it was invented by Italian engineer Luigi Di Ponti in 1933 [3][4][5] who sold the patent to Alfonso Bialetti, an aluminum vendor. It quickly became one of...

Brazilian jiu-jitsu practitioner from Brazil Alessandra VieiraVieira in May 2022BornAlessandra Vieira de Souza[1] (1976-03-14) March 14, 1976 (age 48)São Pedro dos Ferros Minas Gerais, BrazilOther namesAlessandra Vieira Jamgochian[2]NicknameLeka[1]ResidenceValencia, CaliforniaNationalityBrazilian / AmericanDivisionFeathereweightStyleBrazilian Jiu-JitsuTeamCheckmatGracie HumaitáDojo/MachadoRank6th deg. BJJ black belt[a]OccupationBJJ instructorWebsitechec...

John Ernest IAdipati Sachsen-WeimarBerkuasa1605–1620PendahuluJohannPenerusWilhelmInformasi pribadiKelahiran(1594-02-21)21 Februari 1594AltenburgKematian6 Desember 1626(1626-12-06) (umur 32)Sankt Martin, HungariaWangsaWangsa WettinAyahJohann, Adipati Sachsen-WeimarIbuDorothea Maria dari AnhaltAgamaLutheran Johann Ernst I, Adipati Sachsen-Weimar (21 Februari 1594 – 6 Juli 1626), adalah adipati Sachsen-Weimar. Ia adalah anak sulung John II, Adipati Sachsen-Weimar dan Dorot...

Canadian politician (born 1970) The HonourableHarjit SajjanPC OMM MSM CD MPSajjan in 2023President of the King's Privy Council for CanadaIncumbentAssumed office July 26, 2023Prime MinisterJustin TrudeauPreceded byBill BlairMinister of Emergency PreparednessIncumbentAssumed office July 26, 2023Prime MinisterJustin TrudeauPreceded byBill BlairMinister responsible for the Pacific Economic Development Agency of CanadaIncumbentAssumed office October 26, 2021Prime Minist...

This article needs additional citations for verification. Please help improve this article by adding citations to reliable sources. Unsourced material may be challenged and removed.Find sources: Order of British India – news · newspapers · books · scholar · JSTOR (June 2012) (Learn how and when to remove this message) AwardOrder of British IndiaInsignia of the Order, Second Class (above) and First Class, prior to 1939, (below)TypeOrder of meritAwarded...

ХристианствоБиблия Ветхий Завет Новый Завет Евангелие Десять заповедей Нагорная проповедь Апокрифы Бог, Троица Бог Отец Иисус Христос Святой Дух История христианства Апостолы Хронология христианства Раннее христианство Гностическое христианство Вселенские соборы Н...

Metro station in Shenzhen, China This article does not cite any sources. Please help improve this article by adding citations to reliable sources. Unsourced material may be challenged and removed.Find sources: Zhuguang station – news · newspapers · books · scholar · JSTOR (March 2019) (Learn how and when to remove this message) Not to be confused with Zhuguang Road station, a station in Shanghai, China. Zhuguang珠光General informationLocationNanshan ...

يفتقر محتوى هذه المقالة إلى الاستشهاد بمصادر. فضلاً، ساهم في تطوير هذه المقالة من خلال إضافة مصادر موثوق بها. أي معلومات غير موثقة يمكن التشكيك بها وإزالتها. (فبراير 2016) اتحاد جيبوتي لكرة القدم الاسم المختصر FDF الرياضة كرة القدم أسس عام 1979 الانتسابات الفيفا : 1994 الاتحاد ال...

British Conservative politician The subject of this article is standing for re-election to the House of Commons of the United Kingdom on 4 July, and has not been an incumbent MP since Parliament was dissolved on 30 May. Some parts of this article may be out of date during this period. Please feel free to improve this article (but note that updates without valid and reliable references will be removed) or discuss changes on the talk page. Eddie HughesMPOfficial portrait, 2019Parliame...

Bridge in Delhi, IndiaSignature BridgeThe Signature Bridge during construction phaseCoordinates28°42′19″N 77°14′02″E / 28.7053°N 77.2340°E / 28.7053; 77.2340CrossesRiver YamunaLocaleDelhi, IndiaOfficial nameSignature BridgeMaintained byDelhi Tourism and Transportation Development Corporation (DTTDC)CharacteristicsDesignCantilever spar cable-stayed bridgeMaterialSteel and ConcreteTotal length675 metres (2,215 ft)Width35.2 metres (115 ft)Height165 ...

John SheehanSheehan pada 1917Lahir(1885-10-22)22 Oktober 1885Oakland, California, Amerika SerikatMeninggal14 Februari 1952(1952-02-14) (umur 66)Calabasas, California, Amerika SerikatMakamHoly Cross Cemetery, Culver City, CaliforniaPekerjaanPemeranTahun aktif1914–1952Suami/istriBlanche Morris Roberts (m. 19??)Anak2 John Sheehan (22 Oktober 1885 – 14 Februari 1952) adalah seorang pemeran dan pementas vaudeville asal Amerika Serikat. Setelah berakting di atas panggun...

This article has multiple issues. Please help improve it or discuss these issues on the talk page. (Learn how and when to remove these template messages) The topic of this article may not meet Wikipedia's notability guideline for music. Please help to demonstrate the notability of the topic by citing reliable secondary sources that are independent of the topic and provide significant coverage of it beyond a mere trivial mention. If notability cannot be shown, the article is likely to be merg...

Not to be confused with King's Cove, Newfoundland and Labrador. This article is about the town in Newfoundland and Labrador. For other uses, see Kings Point (disambiguation). This article needs additional citations for verification. Please help improve this article by adding citations to reliable sources. Unsourced material may be challenged and removed.Find sources: King's Point – news · newspapers · books · scholar · JSTOR (April 2022) (Learn how and...

Private university in Nashville, Tennessee, US Vandy redirects here. For other uses, see Vandy (disambiguation). Vanderbilt UniversityLatin: Universitas Vanderbiltia[1]Former nameCentral University(1873–1877)MottoCrescere aude (Latin)[2]Motto in EnglishDare to grow[2]TypePrivate research universityEstablished1873; 151 years ago (1873)AccreditationSACSAcademic affiliationsAAUCOFHENAICU[3]ORAUURASpace-grantEndowment$10.2 billion (2022) ...

Lokasi Bono di Craighead County (bawah) dan Arkansas (atas). Untuk kegunaan lain, lihat Bono. Bono adalah kota yang terletak di Craighead County, Arkansas, Amerika Serikat. Demografi Menurut sensus tahun 2000, Bono berpenduduk 1.512 jiwa. Pada tahun 2006, jumlah penduduknya menjadi 1.552 jiwa menurut Biro Sensus Amerika Serikat, bertambah 40 jiwa (2,6%). Geografi Menurut United States Census Bureau, luas Bono adalah 3,7 km², di mana keseluruhannya berupa tanah. Bono terletak sekitar 119...

Диакритические знаки со сходным начертанием: ˇ · ੱ · ◌ﬞЗапросы «Ĭ» и «Ĕ» перенаправляются сюда. На эти темы нужно создать отдельные статьи. Кратка ◌̆˘ Изображение ◄ ◌̂ ◌̃ ◌̄ ◌̅ ◌̆ ◌̇ ◌̈ ◌̉ ◌̊ ► ◄ ˔ ˕ ˖ ˗ ˘ ˙ ˚ ˛ ˜ ► Характеристики Название ◌̆: combining bre...

1. Klasse 1920-1921 Competizione Fußball-Bundesliga Sport Calcio Edizione 10ª Organizzatore ÖFB Luogo Austria Partecipanti 13 Cronologia della competizione 1919-20 1921-22 Manuale L'edizione 1920-21 della Erste Klasse vide la vittoria finale del Rapid Vienna. Capocannoniere del torneo fu Josef Uridil (Rapid Vienna), con 35 reti. Indice 1 Squadre partecipanti 2 Classifica finale 2.1 Verdetti 3 Risultati 3.1 Calendario 4 Collegamenti esterni Squadre partecipanti Admira Vienna &#...

Tragedy written by Jean Racine AndromaqueTitle page from 1668 edition of AndromaqueWritten byJean RacineCharactersAndromaque Pyrrhus Oreste Hermione Pylade Cléone Céphise PhoenixSettingThe Royal Palace at Bouthroton in Epirus Andromaque is a tragedy in five acts by the French playwright Jean Racine written in alexandrine verse. It was first performed on 17 November 1667 before the court of Louis XIV in the Louvre in the private chambers of the Queen, Marie Thérèse, by the royal company of...

هذه المقالة عن سالك التصوف. لمعانٍ أخرى، طالع تصوف (توضيح). السالك السالك هو الذي مشى على المقامات بحاله لا بعلمه وتصوره، فكان العلم الحاصل له عينًا يأبى من ورود الشبهة المضلة له.[1]جزء من سلسلة مقالات عن نزارية-إسماعيلية باطنية، حروفية، كيسانية وشيعة اثنا عشريةال...

English politician Thomas Fanshawe Sir Thomas Fanshawe (1628–1705) was an English politician. Life He was the son of Thomas Fanshawe of Jenkins and his wife, Susan, daughter of Matthias Otten of Putney.[1][2] In the West of England as a royalist of the First English Civil War with his father, in 1645–6, and arrested in 1659, Fanshawe was knighted in 1660 after the English Restoration.[3] He held the post of Clerk of the Crown in the King's Bench, as his father had ...
![The General Scheme for the Hiyama Coupling {\displaystyle {\ce {R-SiR''_{3}+R'-X->[\mathrm {F^{-}} ][{\text{Pd cat.}}]R-R'}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/61136e624b1d2eaf1122ba069be1188b853693be)