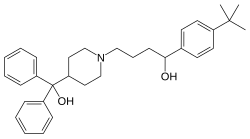
Terfenadin
Terfenadin adalah antihistamin yang dulunya digunakan untuk mengobati kondisi alergi. Obat ini dipasarkan oleh Hoechst Marion Roussel (sekarang Sanofi) dan dipasarkan dengan berbagai nama merek termasuk Seldane di Amerika Serikat, Triludan di Britania Raya, dan Teldane di Australia.[1] Obat ini digantikan oleh feksofenadin pada tahun 1990-an karena risiko gangguan jenis tertentu pada ritme listrik jantung (khususnya aritmia jantung yang disebabkan oleh perpanjangan interval QT) dan telah ditarik dari pasaran di seluruh dunia.[2] SejarahTerfenadin disintesis oleh ahli kimia di Richardson–Merrell pada tahun 1973 sebagai obat penenang yang potensial. Namun, obat ini ditemukan tidak aktif untuk tujuan tersebut karena tidak melewati sawar darah otak atau memasuki sistem saraf pusat. Farmakolog Richard Kinsolving memperhatikan bahwa terfenadin menunjukkan kemiripan struktural dengan antihistamin difenhidramin, sehingga terfenadin diuji sebagai antihistamin. Obat ini ditemukan sebagai antihistamin non-sedatif.[3] Di Amerika Serikat, terfenadin (sebagai Seldane) dipasarkan pada tahun 1985 sebagai antihistamin non-sedatif pertama untuk pengobatan rinitis alergi.[1][4] Pada bulan Juni 1990, bukti adanya aritmia ventrikel yang serius di antara mereka yang mengonsumsi Seldane mendorong FDA untuk mengeluarkan laporan tentang faktor risiko yang terkait dengan penggunaan obat tersebut secara bersamaan dengan antibiotik makrolida dan ketokonazol. Dua bulan kemudian, FDA mengharuskan produsen untuk mengirim surat kepada semua dokter, memberi tahu mereka tentang masalah tersebut; pada bulan Juli 1992, tindakan pencegahan yang ada ditingkatkan menjadi peringatan kotak hitam dan masalah tersebut menarik perhatian media massa dalam laporan bahwa orang dengan penyakit hati atau yang mengonsumsi ketokonazol, atau antibiotik eritromisin, dapat menderita aritmia jantung jika mereka juga mengonsumsi Seldane.[1][4] Pada bulan Januari 1997, bulan yang sama ketika Badan Pengawas Obat dan Makanan Amerika Serikat (FDA) sebelumnya menyetujui versi generik Seldane yang dibuat oleh IVAX Corporation of Miami, FDA merekomendasikan obat yang mengandung terfenadin untuk ditarik dari pasaran dan dokter mempertimbangkan pengobatan alternatif untuk pasien mereka.[4] Seldane dan Seldane-D (terfenadin yang dikombinasikan dengan pseudoefedrin) ditarik dari pasaran AS oleh produsennya pada akhir tahun 1997 setelah FDA menyetujui Allegra-D (feksofenadin/pseudoefedrin).[5] Obat-obatan yang mengandung terfenadin kemudian ditarik dari pasaran Kanada pada tahun 1999,[6] dan tidak lagi tersedia untuk resep di Britania Raya.[7] FarmakologiTerfenadin bekerja sebagai antihistamin selektif perifer, atau antagonis reseptor histamin H1.[3] Obat ini adalah bakal obat, yang umumnya dimetabolisme secara lengkap menjadi bentuk aktif feksofenadin di hati oleh enzim sitokrom P450 3A4. Karena metabolismenya yang hampir lengkap oleh hati segera setelah meninggalkan usus, terfenadin biasanya tidak terukur dalam plasma. Namun, terfenadin sendiri bersifat kardiotoksik pada dosis yang lebih tinggi, sedangkan metabolit aktif utamanya tidak. Selain efek antihistaminnya, terfenadin juga bekerja sebagai penghambat saluran kalium (Kv11.1 yang dikodekan oleh gen hERG). Karena metabolit aktifnya bukan penghambat saluran kalium, tidak ada kardiotoksisitas yang dikaitkan dengan feksofenadin.[8] Toksisitas mendadak mungkin terjadi bahkan setelah bertahun-tahun penggunaan tanpa masalah sebagai akibat dari interaksi dengan obat lain seperti eritromisin, atau makanan seperti jeruk limau gedang. Penambahan atau peningkatan dosis penghambat CYP3A4 ini mempersulit tubuh untuk memetabolisme dan membuang terfenadin. Dalam konsentrasi plasma yang lebih besar, hal ini dapat menyebabkan efek toksik pada ritme jantung (misalnya takikardia ventrikel dan torsade de pointes). Referensi
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||