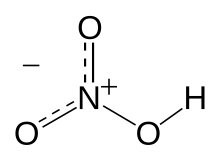
Валентность
|
Read other articles:

I Gusti Gde Raka I Gusti Gde Raka adalah seorang politikus Indonesia. Pada masa pendudukan Hindia Belanda oleh Jepang, ia bekerja pada bagian Kemakmuran dan kemudian pada Perbendaharaan. Pada bulan September 1945, ia diangkat sebagai Kepala Perbendaharaan Provinsi Sunda Kecil Pemerintah Republik Indonesia. Dari Maret 1946 sampai Juli 1949, ia ditawan oleh tentara Belanda. Pada bulan Juli 1949, ia dilepaskan, berangkat ke Jogjakarta dan bekerja sebagai ahli Kepala Keuangan pada Kementerian Keu...

Baronang susu Siganus fuscescens Status konservasiRisiko rendahIUCN69689554 TaksonomiKerajaanAnimaliaFilumChordataKelasActinopteriOrdoPerciformesFamiliSiganidaeGenusSiganusSpesiesSiganus fuscescens Tata namaSinonim takson Centrogaster fuscescens Houttuyn, 1782 Amphacanthus fuscescens (Houttuyn, 1782) Teuthis fuscescens (Houttuyn, 1782) Amphacanthus ovatus Marion de Procé, 1822 Amphacanthus nebulosus Quoy & Gaimard, 1825 Siganus nebulosus (Quoy & Gaimard, 1825) Teuthis nebulosa (Quoy ...

Artikel ini perlu diterjemahkan dari bahasa Melayu ke bahasa Indonesia. Artikel ini ditulis atau diterjemahkan secara buruk dari Wikipedia bahasa Melayu. Jika halaman ini ditujukan untuk komunitas bahasa Melayu, halaman itu harus dikontribusikan ke Wikipedia bahasa Melayu. Lihat daftar bahasa Wikipedia. Artikel yang tidak diterjemahkan dapat dihapus secara cepat sesuai kriteria A2. Jika Anda ingin memeriksa artikel ini, Anda boleh menggunakan mesin penerjemah. Namun ingat, mohon tidak menyali...

1942–43 Penn State Nittany Lions men's ice hockey seasonRecordOverall2–2–0Road1–2–0Neutral1–0–0Coaches and captainsHead coachArthur DavisCaptain(s)Ted CauffmanPenn State Nittany Lions men's ice hockey seasons« 1941–42 1943–44 » The 1942–43 Penn State Nittany Lions men's ice hockey season was the 4th season of play for the program. The Nittany Lions represented Pennsylvania State University and were coached by Arthur Davis in his 3rd season. Season With Worl...

1996 film directed by Brian Henson This article is about the film. For the video game, see Muppet Treasure Island (video game). Muppet Treasure IslandTheatrical release poster by Drew StruzanDirected byBrian HensonScreenplay by Jerry Juhl Kirk R. Thatcher James V. Hart Based onTreasure Islandby Robert Louis StevensonProduced by Brian Henson Martin G. Baker Starring Kevin Bishop Tim Curry Dave Goelz Steve Whitmire Jerry Nelson Kevin Clash Bill Barretta Frank Oz CinematographyJohn FennerEdited ...

Disambiguazione – Se stai cercando altri significati, vedi Gavi (disambigua). Gavicomune Gavi – VedutaGavi vista dal forte LocalizzazioneStato Italia Regione Piemonte Provincia Alessandria AmministrazioneSindacoCarlo Massa (Lista Civica SìAmoGavi) dal 22-9-2020 TerritorioCoordinate44°41′19″N 8°48′37″E / 44.688611°N 8.810278°E44.688611; 8.810278 (Gavi)Coordinate: 44°41′19″N 8°48′37″E / 44.688611°N 8.810278...

Japanese actor Tasuku Emoto柄本 佑Emoto at the 36th Tokyo International Film Festival in October 2023Born (1986-12-16) December 16, 1986 (age 37)Tokyo, JapanEducationWako High SchoolWaseda University Art SchoolOccupationActorYears active2003–presentAgentAlpha AgencyKnown forAsa ga KitaUtsukushī Natsu KirishimaSpouse Sakura Ando (m. 2012)Children1ParentsAkira Emoto (father)Kazue Tsunogae (mother)RelativesTokio Emoto (brother)Eiji Okuda (fath...

Pour les articles homonymes, voir Academia (homonymie). Cet article est une ébauche concernant Taïwan. Vous pouvez partager vos connaissances en l’améliorant (comment ?) selon les recommandations des projets correspondants. Academia sinicaHistoireFondation 9 juin 1928CadreType Académie des sciencesSiège District de Nangang (Taïwan) (depuis 1949)Pays TaïwanCoordonnées 25° 02′ 32″ N, 121° 36′ 52″ EOrganisationSite web www.sinica.edu....

Nachtjagdgeschwader 100Active1943 – 1945Country Nazi GermanyBranch LuftwaffeTypeNight FighterRoleAir superioritySizeAir Force WingEngagementsWorld War IIInsigniaIdentificationsymbolGeschwaderkennung of8V (4.Staffel)Military unit Nachtjagdgeschwader 100 (NJG 100) was a Luftwaffe night fighter-wing of World War II. The Geschwader did not have a Stab and no Geschwaderkommodore. It had two Gruppen (groups), operating separately. The I. Gruppe of NJG 100 was formed in early 1943 from t...

Questa voce sull'argomento cestisti statunitensi è solo un abbozzo. Contribuisci a migliorarla secondo le convenzioni di Wikipedia. Segui i suggerimenti del progetto di riferimento. Justin Wright-Foreman Nazionalità Stati Uniti Altezza 188 cm Peso 86 kg Pallacanestro Ruolo Playmaker Squadra V.L. Pesaro Carriera Giovanili High School for Construction2015-2019 Hofstra Pride Squadre di club 2019-2020 Utah Jazz4 (19)2019-2020→ S.L.C. Stars36 (621)2021 Er...

Disambiguazione – Se stai cercando il conte di Moray, vedi Giacomo Stewart (conte di Moray). Disambiguazione – Se stai cercando il duca di Ross, vedi Giacomo Stewart, duca di Ross. Regno di ScoziaStuart Roberto II Figli Margherita Giovanni Walter Roberto Marjory Giovanna Isabella Elisabetta Walter Elisabetta Caterina Egidia Roberto III Figli Elisabetta Margherita Maria Davide Giacomo I Giovanni Giacomo I Figli Margherita Isabella Eleonora Giovanna Alessandro Giacomo Maria Annabella Giaco...

Peta menunjukan lokasi Jones Data sensus penduduk di Jones Tahun Populasi Persentase 199534.669—200039.0012.56%200741.2370.77% Jones adalah munisipalitas yang terletak di provinsi Isabela, Filipina. Pada tahun 2010, munisipalitas ini memiliki populasi sebesar 45.422 jiwa atau 10.198 rumah tangga. Pembagian wilayah Secara administratif Jones terbagi menjadi 42 barangay, yaitu: Abulan Addalam Arubub Bannawag Bantay Barangay I (Pob - Centro) Barangay II (Pob.) Barangcuag Dalibubon Daligan Diar...

American professional soccer club Soccer clubChicago Red StarsFounded2006; 18 years ago (2006)StadiumSeatGeek StadiumBridgeview, IllinoisCapacity20,000Majority ownerLaura RickettsChairpersonLaura RickettsHead coachLorne DonaldsonLeagueNational Women's Soccer League2023Regular season: 12th of 12Playoffs: DNQWebsiteClub website Home colors Away colors Current season The Chicago Red Stars are a professional women's soccer club based in Bridgeview, Illinois, a suburb of Chicago....

Termination of a marital union This article is about dissolution of marriage. For other uses, see Divorce (disambiguation). Divorcee redirects here. For other uses, see Divorcee (disambiguation). This article has multiple issues. Please help improve it or discuss these issues on the talk page. (Learn how and when to remove these template messages) This article needs additional citations for verification. Please help improve this article by adding citations to reliable sources. Unsourced mater...

У этого термина существуют и другие значения, см. Октябрь (значения). ←→Октябрь Пн Вт Ср Чт Пт Сб Вс 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 2024 год Октя́брь (от лат. octō — восемь) — десятый месяц Григорианского календаря. Восьмой месяц старорим�...

У этого термина существуют и другие значения, см. Брат. Эта статья — о российском фильме 1997 года. О советском фильме 1982 года см. Брат (фильм, 1982). Брат Жанр криминальная драма Режиссёр Алексей Балабанов Продюсер Сергей Сельянов Авторсценария Алексей Балабанов В&#...

Japanese light novel series For the web novel series by Hanyuu, see Hazure Skill Kinomi Master. Hazure Skill: The Guild Member with a Worthless Skill is Actually a Legendary AssassinCover of the first light novel volume外れスキル「影が薄い」を持つギルド職員が、実は伝説の暗殺者(Hazure Sukiru Kage ga Usui o Motsu Guild Shokuin ga, Jitsuha Densetsu no Ansatsusha)GenreFantasy[1] Novel seriesWritten byKennojiPublished byShōsetsuka ni NarōOriginal ru...

Samsung Gear LiveDeveloperSamsung ElectronicsProduct familyGearTypeSmartwatchRelease dateJune 25, 2014 (2014-06-25)DiscontinuedMay 14, 2015 (Google Store)Operating systemAndroid Wear 4.4.2System on a chipQualcomm Snapdragon 400 MSM8226CPUQuad-core 1.2 GHzMemory512 MBStorage4 GBDisplay1.63 in (41 mm) Super AMOLED with RGB matrix320×320 pixels (1:1 Aspect ratio) (278 ppi)ConnectivityBluetooth SmartPower300 mAhOnline servicesGoogle Play, Google NowMass59&...
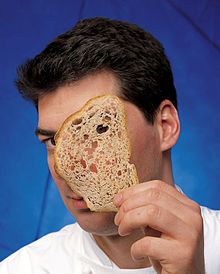
Lo chef Massimiliano Alajmo nel 2008, fotografato da Wowe Massimiliano Alajmo (Padova, 6 maggio 1974) è un cuoco italiano. Indice 1 Biografia 2 Opere 3 Note 4 Bibliografia 5 Voci correlate 6 Altri progetti 7 Collegamenti esterni Biografia Appartenente ad un'antica famiglia di ristoratori veneti, dopo il conseguimento del diploma dell'istituto tecnico alberghiero ad Abano Terme, nel 1990 approfondisce la sua esperienza presso il ristorante “Ja Navalge” di Alfredo Chiocchetti a Moena, nel ...

Private university in Lexington, Virginia, US Washington and Lee redirects here. For the school in Montross, Virginia, see Washington and Lee High School. For the school in Arlington, Virginia, see Washington-Liberty High School. Washington and Lee UniversityWashington and Lee University coat of armsFormer namesAugusta Academy(1749–1776)Liberty Hall Academy(1776–1796)Washington Academy(1796–1813)Washington College(1813–1870)MottoLatin: Non Incautus FuturiMotto in EnglishNot Unmin...