|
Квантовая химияКва́нтовая хи́мия — направление теоретической химии, рассматривающее строение и свойства химических соединений, реакционную способность, кинетику и механизм химических реакций на основе квантовой механики[1]. Разделами квантовой химии являются: квантовая теория строения молекул, квантовая теория химических связей и межмолекулярных взаимодействий, квантовая теория химических реакций и реакционной способности и др.[2] Она занимается рассмотрением химических и физических свойств веществ на атомарном уровне (моделях электронно-ядерного строения и взаимодействий, представленных с точки зрения квантовой механики). Вследствие того, что сложность изучаемых объектов во многих случаях не позволяет находить явные решения уравнений, описывающих процессы в химических системах, применяют приближенные методы расчета. С квантовой химией неразрывно связана вычислительная химия — дисциплина, использующая математические методы квантовой химии, адаптированные для создания специальных компьютерных программ, используемых для расчета молекулярных свойств, амплитуды вероятности нахождения электронов в атомах, симуляции взаимодействия молекул. Общие сведенияОсновной задачей квантовой химии является решение уравнения Шрёдингера и его релятивистского варианта (уравнение Дирака) для атомов и молекул. Уравнение Шрёдингера решается аналитически лишь для немногих систем (например, для моделей типа жёсткий ротатор (модель, описывающая линейные молекулы с постоянным межъядерным расстоянием, в такой модели уровни энергии зависят только от вращательного квантового числа), гармонический осциллятор, одноэлектронная система). Реальные многоатомные системы содержат большое количество взаимодействующих электронов, а для таких систем не существует аналитического решения этих уравнений, и, по всей видимости, оно не будет найдено и в дальнейшем. По этой причине в квантовой химии приходится строить различные приближённые решения. Из-за быстрого роста сложности поиска решений с ростом сложности системы и требований к точности расчёта, возможности квантовохимических расчётов сильно ограничиваются текущим развитием вычислительной техники, хотя, наблюдаемые в последние два десятилетия революционные сдвиги в развитии компьютерной техники, приведшие к её заметному удешевлению, заметно стимулируют развитие прикладной квантовой химии. Решение уравнения Шрёдингера часто строится на уравнении Хартри — Фока — Рутана итерационным методом (SCF-self consistent field — самосогласованное поле) и состоит в нахождении вида волновой функции. Приближения, используемые в квантовой химии:
где Ψ(r) — молекулярная орбиталь, ci — коэффициент вхождения (амплитуда вероятности) i-той атомной орбитали в молекулярную орбиталь, ψi — волновая функция i-той атомной орбитали (получается при решении уравнения Шрёдингера для водородоподобного атома — известно в точном виде). Решение задачи состоит в нахождении коэффициентов сi. При учёте всех интегралов — так называемый метод Ab initio — количество вычислений растёт пропорционально количеству электронов в 6—8 степени, при полуэмпирических методах — в 4—5 степени. Получаемая при решении уравнения волновая функция описывает чистое квантовое состояние системы. Квадрат модуля волновой функции характеризует плотность вероятности обнаружения системы в заданной точке конфигурационного пространства. Эту интерпретацию впервые предложил Макс Борн, которому за фундаментальные исследование в области квантовой механики, в частности за статистическую (вероятностную) интерпретацию волновой функции, в 1954 году была присуждена Нобелевская премия по физике. Строение атома А́том (от др.-греч. ἄτομος — неделимый) — наименьшая часть химического элемента, являющаяся носителем его свойств[3]. Атом состоит из атомного ядра и электронов. При этом порядковый номер элемента (Z) соответствует числу протонов (Z) в атомном ядре, определяет суммарный положительный электрический заряд (Ze) атомного ядра, несущего почти всю массу атома (более чем 99,9 %), а также число электронов (Z) в нейтральном атоме, определяющих его размер[4]. Электроны образуют электронную оболочку атома. Заполнение электронных оболочек подчиняется принципу Паули — в атоме не может быть двух электронов (принцип запрета Паули относится к фермионам, электроны таковыми и являются), имеющих одинаковый набор всех четырёх квантовых чисел. Ёмкость уровней электронных оболочек по мере удаления от ядра увеличивается и составляет 2 (n = 1), 8 (n = 2), 18 (n = 3), 32 (n = 4) и т. д. электронов. Слои электронных оболочек с главным квантовым числом {{{1}}} обозначаются соответственно прописными буквами K, L, M, N… Порядок заполнения подслоя электронных оболочек подчиняется правилу Хунда — суммарное спиновое число электронов данного подслоя должно быть максимальным. Распределение электронов в атомах называют электронной конфигурацией. Электронная конфигурация обозначается при помощи показателей степени, которые указывают число электронов на электронной оболочке 1s, 2s, 2p и т. д. Буквы s, p, d, f символизируют последовательные значения орбитального квантового числа l (l соответственно равно 0, 1, 2, 3)[5]. Согласно представлениям квантовой механики, атомы не имеют определённых границ, однако вероятность найти электрон, связанный с данным ядром, на расстоянии r от ядра быстро падает с увеличением r. Поэтому атому можно приписать некоторый размер[6]. Радиальная функция распределения вероятности нахождения электрона в атоме водорода обладает максимум при α0, как показано на рис. 1. Этот наиболее вероятный радиус для электрона совпадает с боровским радиусом. Более размытое облако плотности вероятности, полученные при квантовомеханическом рассмотрении, значительно отличается от боровской модели атома и согласуется с принципом неопределённости Гейзенберга[7]. Лучшим описанием эффективных размеров изолированного атома является теоретически рассчитанное положение его наружных электронов. Это так называемый орбитальный радиус атома. В зависимости от порядкового номера элемента (Z) проявляется чёткая периодичность в изменении значений орбитальных атомных радиусов[8]. Размер электронной оболочки атома более чем в 10 тысяч раз превышает размер его атомного ядра. Ядро атома состоит из положительно заряженных протонов и незаряженных нейтронов. Если число протонов в ядре совпадает с числом электронов, то атом в целом оказывается электрически нейтральным. В противном случае он обладает некоторым положительным или отрицательным зарядом и называется ионом. Атомы классифицируются по количеству протонов и нейтронов в ядре: количество протонов определяет принадлежность атома некоторому химическому элементу, а сумма числа нейтронов и протонов — изотопу этого элемента. Образование химической связи и строение молекул и твёрдых телЕдинственной молекулярной системой, для которой уравнение Шрёдингера может быть решено аналитически, является молекулярный ион водорода H2+, где единственный электрон движется в поле двух ядер (протонов). Длина химической связи в молекулярном ионе водорода H2+ составляет 1,06 Å. Энергия разрыва химической связи в молекулярном ионе водорода H2+ составляет 61 ккал/моль. Энергия притяжения электрона к обоим ядрам в одноэлектронной химической связи компенсирует энергию отталкивания протонов, которая на расстоянии 1,06 Å составляет 314 ккал/моль. H + H+ → H2+ + 61 ккал/моль[9]. Поскольку точное решение уравнения Шрёдингера для атомно-молекулярных систем, содержащих более одного электрона, невозможно, возник ряд приближённых теорий химической связи.
В 1958 г. на симпозиуме по теоретической органической химии, посвящённой памяти А.Кекуле, Полинг представил теорию изогнутой химической связи. Двойная и тройная химическая связь рассматривалась, как комбинация двух или трёх изогнутых одинарных связей[10]. Правила равного удаления электронов друг от друга непосредственно следует из закона Кулона, согласно которому электроны стремятся находиться на максимально удалённом расстоянии друг от друга. Например, молекулы типа BeH2 имеют строго линейную конфигурацию. Атомы III группы таблицы Менделеева образуют тригональные молекулы, типа BF3. Атомы IV группы образуют тетраэдрические молекулы, типа CH4. Молекулы, образованные атомами V и VI групп, имеют геометрию тригональной бипирамиды и октаэдра, соответственно[11]. Физические, в том числе спектральные свойства атомов, молекул и твёрдых телЭмиссионный спектрКвантование энергии атомов проявляется в их спектрах поглощения (абсорбиционные спектры) и испускания (эмиссионные спектры). Атомные спектры имеют линейчатый характер (рис. 2). 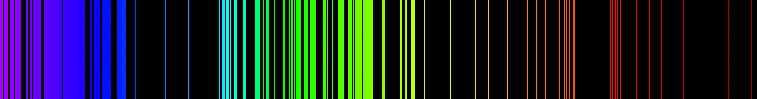 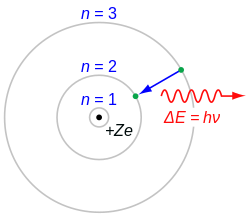 Возникновение линий в спектре обусловлено тем, что при возбуждении атомов электроны, принимая соответствующую порцию энергии, переходят на более высокий энергетический уровень. Переход электронов в состояние с более низким энергетическим уровнем сопровождается выделением кванта энергии (рис. 3). Наиболее простой спектр у атома водорода, линии которого образуют спектральные серии; их положение описывается выражением ν = R (1/n12 — 1/n22), где ν — волновое число линии, R — постоянная Ридберга, n — целые числа, причём n2 > n1.
Аналогичные серии наблюдаются в спектрах водородоподобных ионов (например, He+, Li2+). С увеличением числа электронов атомные спектры усложняются и закономерности в расположении линий становятся менее выраженными. Поляризуемость атомов и молекул Внешнее электрическое поле напряжённостью , наложенное на систему взаимодействующих ядер и электронов (атомов, ионов, молекул), деформирует её, вызывая появление наведённого дипольного момента где коэффициент имеет размерность объёма и является количественной мерой электронной поляризуемости (его также называют электронной поляризуемостью). На рис. 4 представлена деформационная поляризация (смещение электронной оболочки) атома водорода под действием электрического поля протона. При снятии внешнего электрического поля наведённый дипольный момент исчезает. В случае взаимодействия атома водорода и протона имеет место образование молекулярного иона водорода с простейшей одноэлектронной химической связью:
Относительно недавно были получены достоверные данные по электронным поляризуемостям большинства атомов в свободном состоянии. Наибольшее значение электронной поляризуемости наблюдается у атомов щелочных металлов, а минимальное — у атомов инертных газов[12]. В случае многоядерных систем внешнее электрическое поле приводит как к деформации электронных оболочек, так и изменению равновесных расстояний между ядрами (длины связи). В соответствии с этим поляризуемость молекулы составляется из двух слагаемых: где электронная поляризуемость, атомная поляризуемость[13]. Ионизация атомов и молекулПри высокой напряжённости внешнего электрического поля, наложенного на систему взаимодействующих ядер и электронов происходит её ионизация — отрыв электрона от атома или молекулы и образование положительно заряженного иона — катиона. Процесс образования ионов из атомов или молекул всегда эндотермический. Количество энергии, необходимое для отрыва электрона от возбуждаемых атомов или молекул, принято называть энергией ионизации. Для многоэлектронных атомов энергия ионизации l1, l2, l3… соответствует отрыву первого, второго, третьего и т. д. электронов. При этом всегда l1 < l2 < l3…, так как увеличение числа оторванных электронов приводит к возрастанию положительного заряда образующегося иона. Наименьшей энергией ионизации (3—5 эВ) обладают атомы щелочных металлов, имеющих по одному валентному электрону, наибольшей — атомы инертных газов, обладающих замкнутой электронной оболочкой. В связи с низкими значениями энергии ионизации щелочных металлов атомы их под влиянием различных воздействий сравнительно легко теряют свои внешние электроны. Такая потеря происходит под действием освещения чистой поверхности щелочного металла. На этом явлении, которое носит название фотоэлектрического эффекта, основано действие фотоэлементов, то есть приборов, непосредственно трансформирующих световую энергию в электрическую[14]. Квантовая природа фотоэлектрического эффекта установлена Эйнштейном, которому присуждена в 1921 году Нобелевская премия за труды по теоретической физике, особенно за открытие законов фотоэффекта. Сродство к электрону  Электрон, обладая отрицательным элементарным зарядом 1,602•10−19 Кл, как и всякий точечный электрический заряд создаёт вокруг себя электрическое поле с напряжённостью где расстояние точки поля до электрона. Атом водорода, попадая в электрическое поле электрона, подвергается деформационной поляризации. Величина наведённого дипольного момента μ, прямо пропорциональна напряжённости электрического поля Величина смещения центра электронной оболочки атома водорода обратно пропорциональна квадрату расстояния атома водорода к приближающемуся электрону (рис. 5). Сближение атома водорода и электрона возможно до тех пор, пока центры областей плотностей вероятности нахождения электронов не станут равноудалёнными от ядра объединённой системы — отрицательно заряженного иона водорода (гидрид-иона ). Энергетический эффект процесса присоединения электрона к нейтральному атому Э принято называть энергией сродства к электрону. В процессе присоединения электрона к нейтральному атому образуется отрицательно заряженный ион (анион) Э–:
На рис. 6 представлена зависимость энергии сродства к электрону атомов от порядкового номера элемента для некоторых элементов. Наибольшим сродством к электрону обладают p-элементы VII группы (галогены). Взаимодействие отдельных молекулМежмолекулярное взаимодействие — это электромагнитное взаимодействие электронов и ядер одной молекулы с электронами и ядрами другой. Межмолекулярное взаимодействие зависит от расстояния R между молекулами и их взаимной ориентации и определяется потенциальной энергией. Энергия притяжения молекул может быть представлена в виде трёх составляющих: ориентационной Еор, индукционной Еинд, и дисперсионной Едисп.[15] См. также* Методы Ab initio
Примечания
Литература
Ссылки
Information related to Квантовая химия |















