CD4
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Read other articles:

English actor This article has multiple issues. Please help improve it or discuss these issues on the talk page. (Learn how and when to remove these template messages) This article has an unclear citation style. The references used may be made clearer with a different or consistent style of citation and footnoting. (September 2009) (Learn how and when to remove this template message) This article's lead section may be too short to adequately summarize the key points. Please consider expanding...

Pour les articles homonymes, voir Vingt-Trois-Août. Éphémérides Août 1er 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 28 29 30 31 23 juillet 23 septembre Chronologies thématiques Croisades Ferroviaires Sports Disney Anarchisme Catholicisme Abréviations / Voir aussi (° 1852) = né en 1852 († 1885) = mort en 1885 a.s. = calendrier julien n.s. = calendrier grégorien Calendrier Calendrier perpétuel Liste de calendriers Naissances d...

Madulain Lambang kebesaranNegaraSwissKantonGraubündenDistrikMalojaLuas[1] • Total16,28 km2 (6,29 sq mi)Ketinggian1.697 m (5,568 ft)Populasi (Kesalahan: waktu tidak sah.[2]) • Total194 • Kepadatan12/km2 (31/sq mi)Kode pos7523Kode area telepon3783Dikelilingi olehBever, La Punt-Chamues-ch, Pontresina, S-chanf, ZuozSitus webwww.madulain.ch SFSO statistics Madulain ([mɐduˈlaɪ̯n]ⓘ) adalah sebuah munisipali...

NASCAR Seri XfinityKategoriBalap mobil stokNegara atau daerahAmerika SerikatMusim pertama1982PabrikanChevrolet · Ford · ToyotaPemasok mesinChevrolet · Ford · ToyotaPemasok banGoodyearJuara pembalapTy GibbsJuara timJoe Gibbs RacingJuara pabrikanToyotaSitus webNASCAR Seri Xfinity Musim saat ini NASCAR Seri Xfinity (sebelumnya NASCAR Seri Busch dan NASCAR Seri Nationwide) merupakan sebuah seri balap mobil stok yang dioperasikan oleh National Association fo...
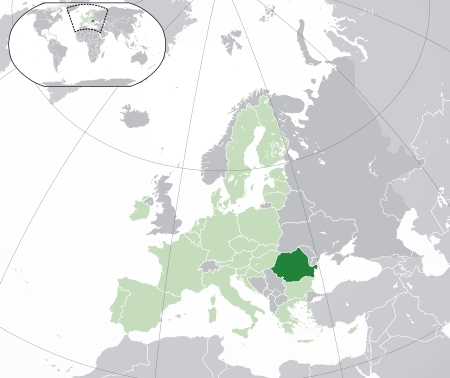
RumaniaRomânia (Rumania) Bendera Lambang Lagu kebangsaan: Deşteaptă-te, române! (Bangunlah, Bangsa Rumania!) Perlihatkan BumiPerlihatkan peta EropaPerlihatkan peta BenderaLokasi Rumania (hijau gelap)– di Eropa (hijau & abu-abu)– di Uni Eropa (hijau)Ibu kota(dan kota terbesar)Bukares44°26′N 26°6′E / 44.433°N 26.100°E / 44.433; 26.100Bahasa resmiRumaniaKelompok etnik (2021)89,3% Rumania6...

تصوف إسباني فرانسيس بورجيا يوحنا الأفيلي تيريزا الأفيلاوية يوحنا الصليب لويس دو ليون إغناطيوس دي لويولا ماریا دو آجریدا لويس دي جونجورا تعديل - تعديل مصدري - تعديل ويكي بيانات التصوف الإسباني هو تصوف مسيحي إزدهر مع حركة الإصلاح الكاثوليكي في القرن السادس عشر والقرن السابع...

Set of processes exchanging nutrients between parts of a system Composting within agricultural systems capitalizes upon the natural services of nutrient recycling in ecosystems. Bacteria, fungi, insects, earthworms, bugs, and other creatures dig and digest the compost into fertile soil. The minerals and nutrients in the soil is recycled back into the production of crops. A nutrient cycle (or ecological recycling) is the movement and exchange of inorganic and organic matter back into the produ...

Bag used by airline passengers in the event of motion sickness Unused airsickness bags of Thai Airways and Lufthansa. Note the metal clips to close bags after use. A sickness bag (also known as a sick sack, airsick bag, airsickness bag, emesis bag, sick bag, barf bag, vomit bag, throw up bag, disposal bag, waste bag, doggie bag, sickness sack or motion sickness bag) is a small bag commonly provided to passengers on board airplanes and boats to collect and contain vomit in the event of motion ...

American computer and video game development company Wahoo Studios, IncCompany typePrivate companyIndustryVideo gamesFounded2001HeadquartersOrem, Utah, USWebsitewww.wahoo.com Wahoo Studios is a computer and video game development company based in Orem, Utah. Founded in 2001, the company largely serves as consultants or on a contract basis working with larger gaming companies such as Electronic Arts and Microsoft. Historically, the development house has mostly been responsible for console game...

7-та окрема механізована бригада Нарукавний знак бригадиНа службі 22 вересня 2004 — травень 2005[1]Країна УкраїнаВид Сухопутні військаТип Механізовані військаЧисельність 1587[2]У складі Багатонаціональна дивізіяЦентр-Південь[en]Базування провінція Васи...

Musée Goethe à l'Auberge au BœufMusée Goethe à l'Auberge au Bœuf, face à l'église luthérienne de SessenheimInformations généralesType Auberge gastronomique, et muséeOuverture 1899Dirigeant Christiane Sautter-GermainSite web www.auberge-au-boeuf.comCollectionsCollections Documents originaux, lettres, poèmes, tableaux... de l’idylle de Goethe et Frédéric entre 1770 et 1771Époque XVIIIe siècleBâtimentProtection Maisons des IllustresLocalisationPays FranceDivision adminis...

Boy Scouts council in Chicago, Illinois, US Pathway to Adventure CouncilOwnerBoy Scouts of AmericaCountryUnited StatesFounded2015Membership9,000 youth6,000 adultsPresidentStephen W. SchwabCouncil CommissionerBertha GuzmanScout ExecutiveJeff Isaac Websitepathwaytoadventure.org Scouting portal Pathway to Adventure Council is a Boy Scouts of America local council headquartered in Chicago, Illinois. Created from the merger of four councils, it now spans over a large portion of Chicago metrop...

Feminist modern witchcraft organization founded in 1979 by Starhawk and Diane Baker This article possibly contains original research. Please improve it by verifying the claims made and adding inline citations. Statements consisting only of original research should be removed. (December 2021) (Learn how and when to remove this message) Part of a series onFeminism History Feminist history History of feminism Women's history American British Canadian German Waves First Second Third Fourth Timeli...

Types of robot sensors (Light and Sound sensors) Sensor robot adalah sensor yang digunakan untuk mengestimasi kondisi dan lingkungan robot. Sinyal ini dilewatkan ke controller untuk memungkinkan perilaku yang sesuai.[1][2] Sensor pada robot didasarkan pada fungsi organ sensorik manusia. Robot membutuhkan informasi yang luas tentang lingkungannya agar berfungsi secara efektif. Jenis-Jenis Sensor Pada Robot Ada banyak sekali jenis sensor yang bisa ditanamkan pada robot. Dengan m...

Disambiguazione – Polanski rimanda qui. Se stai cercando altri significati, vedi Polanski (disambigua). Roman Polański nel 2023 Oscar al miglior regista 2003 Roman Polański, vero nome Rajmund Roman Thierry Polański (Parigi, 18 agosto 1933), è un regista, sceneggiatore, attore e produttore cinematografico polacco naturalizzato francese. Indice 1 Biografia 1.1 Origini e formazione 1.2 Le prime opere in Polonia 1.3 I soggiorni in Francia, Gran Bretagna e le collaborazioni con Gér...

Air warfare branch of the Armed Forces of the Philippines Philippine Air ForceHukbong Himpapawid ng PilipinasSeal of the Philippine Air ForceFoundedJuly 1, 1947; 77 years ago (1947-07-01)Country PhilippinesTypeAir forceRoleAerial warfareSize 17,600 active personnel[1] 16,000 reserve personnel[1] 224 aircraft Part ofArmed Forces of the PhilippinesHeadquartersColonel Jesus Villamor Air Base, Pasay CityMotto(s)Guardians of our Precious Skies, Bearers o...

هذه المقالة يتيمة إذ تصل إليها مقالات أخرى قليلة جدًا. فضلًا، ساعد بإضافة وصلة إليها في مقالات متعلقة بها. (يونيو 2022) لمعانٍ أخرى، طالع الشراقي (توضيح). يفتقر محتوى هذه المقالة إلى الاستشهاد بمصادر. فضلاً، ساهم في تطوير هذه المقالة من خلال إضافة مصادر موثوق بها. أي معلو...

Voce principale: Ravenna Football Club 1913. Associazione Calcio RavennaStagione 1945-1946Sport calcio Squadra Ravenna Allenatore Gastone Prendato Presidente Sante Gondolini Serie C3° Maggiori presenzeCampionato: Alfredo Calderoni e Alessandro Sassi (22) Miglior marcatoreCampionato: Dalle Vacche (11) 1943-1944 1946-1947 Si invita a seguire il modello di voce Questa pagina raccoglie le informazioni riguardanti l'Associazione Calcio Ravenna nelle competizioni ufficiali della stagione 194...

Influential theologians and writers in the 17th-century Anglican Church Charles II was restored as King of England in 1660. Part of a series on theHistory of the Church of EnglandWestminster Abbey (1749) by Canaletto Middle Ages (597–1500)Anglo-Saxon ChristianityReligion in Medieval EnglandConvocations of Canterbury and YorkDevelopment of dioceses Reformation (1509–1559)Reformation ParliamentDissolution of the MonasteriesThomas CranmerBook of Common Prayer (1549)Edwardine OrdinalsBook of ...

This article is about the chemical element. For the software testing framework, see Selenium (software). Chemical element with atomic number 34 (Se)Selenium, 34SeSeleniumPronunciation/sɪˈliːniəm/ (sə-LEE-nee-əm)Appearancegrey metallic-looking, red, and vitreous black (not pictured) allotropesStandard atomic weight Ar°(Se)78.971±0.008[1]78.971±0.008 (abridged)[2] Selenium in the periodic table Hydrogen Helium Lithium Beryllium Boron Carbon Nit...

