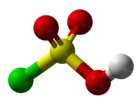
Acide chlorosulfurique
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Read other articles:

American singer and guitarist (1964–2017) Chris CornellCornell in 2011BornChristopher John Boyle(1964-07-20)July 20, 1964Seattle, Washington, U.S.DiedMay 18, 2017(2017-05-18) (aged 52)Detroit, Michigan, U.S.Cause of deathSuicide by hangingResting placeHollywood Forever CemeteryOccupationsSingermusiciansongwriterYears active1983–2017Spouses Susan Silver (m. 1990; div. 2004) Vicky Karayiannis (m. ...

Artikel ini tidak memiliki referensi atau sumber tepercaya sehingga isinya tidak bisa dipastikan. Tolong bantu perbaiki artikel ini dengan menambahkan referensi yang layak. Tulisan tanpa sumber dapat dipertanyakan dan dihapus sewaktu-waktu.Cari sumber: Bata ringan – berita · surat kabar · buku · cendekiawan · JSTOR artikel ini perlu dirapikan agar memenuhi standar Wikipedia. Tidak ada alasan yang diberikan. Silakan kembangkan artikel ini semampu Anda. ...

بدالة الهاتف أو مقسم الهاتف (بالإنجليزية: Telephone exchange) هو نظام اتصال عن بعد يستخدم في الشبكة العامة لتحويل الهاتف أو في المشاريع الكبيرة.المقسم يتألف من مكونات إلكترونية وفي الأنظمة الأقدم كان يستخدم العنصر البشري (كتحويلة) لربط خطوط هواتف المشتركين أو دوائر كهربائية في ال...

Pemberontakan BatipuhMonumen Batipuh di Guguk Malintang, didirikan untuk memperingati tentara yang gugur.Tanggal1841LokasiPantai Barat Sumatra, Sumatera BaratHasil Kemenangan Pemerintah Hindia BelandaPihak terlibat Minangkabau Hindia BelandaTokoh dan pemimpin Tuan Gadang (diasingkan) Kolonel Michiels Pemberontakan Batipuh 1841 merupakan pemberontakan bersenjata rakyat terhadap pemerintahan Hindia Belanda di Batipuh, Pantai Barat Sumatra tahun 1841 yang dipimpin oleh Tuan Gadang. Sebagai...

Red PunchAlbum mini karya Rocket PunchDirilis10 Februari 2020 (2020-02-10)Direkam2019GenreK-popDancepopmoombahtonBalada[1]BahasaKoreanLabelWoollimKronologi Rocket Punch Pink Punch(2019) Red Punch(2020) Blue Punch(2020) Singel dalam album Red Punch BouncyDirilis: 10 Februari 2020 Video musikBouncy di YouTube Red Punch adalah album mini kedua dari grup vokal wanita asal Korea Selatan Rocket Punch. Album ini dirilis secara digital dan fisik pada tanggal 10 Februari 2020 oleh Woo...

Lambang copyleft yang merupakan lambang hak cipta (copyright) yang diputar ke kiri. Copyleft (hak tiru) adalah permainan kata dari copyright (hak cipta) dan seperti halnya makna berlawanan yang dikandung masing-masing (right vs left), begitu pula arti dari kedua istilah tersebut berlawanan. Copyleft merupakan praktik penggunaan undang-undang hak cipta untuk meniadakan larangan dalam pendistribusian salinan dan versi yang telah dimodifikasi dari suatu karya kepada orang lain dan mengharuskan k...

Shaped charge rifle grenade Gewehr-Panzergranate A schematic of components.TypeShaped charge rifle grenadePlace of origin Nazi GermanyService historyUsed byWehrmachtWarsWorld War II[1]SpecificationsMass250 g (8.8 oz)Length160 mm (6.4 in)Diameter30.16 mm (1.1875 in)Muzzle velocity50 m/s (160 ft/s)[2]Maximum firing range46–114 m (50–125 yd)[1]WarheadTNTWarhead weight50 g (1...

Синелобый амазон Научная классификация Домен:ЭукариотыЦарство:ЖивотныеПодцарство:ЭуметазоиБез ранга:Двусторонне-симметричныеБез ранга:ВторичноротыеТип:ХордовыеПодтип:ПозвоночныеИнфратип:ЧелюстноротыеНадкласс:ЧетвероногиеКлада:АмниотыКлада:ЗавропсидыКласс:Пт�...

Australian female goalball Paralympian (born 1990) Tyan Taylor2012 Australian Paralympic team portrait of TaylorPersonal informationNicknameLittle girlNationalityAustralianBorn (1990-03-23) 23 March 1990 (age 34)Height156 cm (61 in) (2012)SportCountryAustraliaSportGoalball Tyan Little Girl Taylor (born 23 March 1990) is an Australian goalball winger and is classified as a B3 competitor. In 2009, after only a month playing the sport, Taylor was named to the New South Wales team....

Ernst TryggerPrime Minister of SwedenIn office19 April 1923 – 18 October 1924MonarchGustaf VPreceded byHjalmar BrantingSucceeded byHjalmar BrantingMinister of Foreign AffairsIn office2 October 1928 – 7 June 1930Prime MinisterArvid LindmanPreceded byEliel LöfgrenSucceeded byFredrik Ramel Personal detailsBorn(1857-10-27)27 October 1857Stockholm, SwedenDied23 September 1943(1943-09-23) (aged 85)Stockholm, SwedenPolitical partyNationalSpouseSigne SöderströmAlma mater...

Di Jepang, Istana Tōgū (東宮code: ja is deprecated , Tōgū, litt. Istana Timur) secara tradisional tidak merujuk ke satu lokasi, tetapi ke kediaman putra Mahkota Kekaisaran. Karena Pangeran Akishino, pewaris saat ini, bukan keturunan pria langsung daru Kaisar dan dirinya sendiri bukan Putra Mahkota Kekaisaran, saat ini tidak ada Istana Tōgū di Jepang dan tidak akan ada satupun sampai ada putra Mahkota Kekaisaran lainnya. Istana Akasaka Istana Akasaka赤坂御所Pintu Samegahashi-mon da...

Сельское поселение России (МО 2-го уровня)Маритуйское муниципальное образование 51°47′09″ с. ш. 104°12′48″ в. д.HGЯO Страна Россия Субъект РФ Иркутская область Район Слюдянский Включает 7 населённых пунктов Адм. центр Маритуй Глава администрации Маритуйского с�...

Tapak Suci Putera MuhammadiyahTipeOrganisasi Pencak SilatKantor pusatpasar baru, Yogyakarta, IndonesiaKetua UmumMuhammad Afnan Hadikusumo Para santri PPTQM Pakan Sinayan, Kabupaten Agam, Sumatera Barat sedang berlatih Tapak Suci Tapak Suci Putera Muhammadiyah, atau disingkat Tapak Suci, adalah sebuah aliran, perguruan, dan organisasi pencak silat yang merupakan anggota Ikatan Pencak Silat Indonesia (IPSI). Tapak Suci termasuk dalam 10 perguruan historis IPSI, yaitu perguruan yang menunjang tu...

Canadian journalist and politician (1950–2023) Not to be confused with David Olney, an American singer-songwriter. The HonourableDavid OnleyCM OOntOnley in 201328th Lieutenant Governor of OntarioIn officeSeptember 5, 2007 – September 23, 2014MonarchElizabeth IIGovernors General Michaëlle Jean David Johnston Premier Dalton McGuinty Kathleen Wynne Preceded byJames BartlemanSucceeded byElizabeth Dowdeswell Personal detailsBornDavid Charles Onley(1950-06-12)June 12, 1950Midl...

Artikel ini bukan mengenai Rubah dan Singa Sakit. Sebuah ilustrasi karya Richard Heighway dari kumpulan fabel tahun 1894 Rubah dan Singa[1][2] adalah salah satu Fabel Aesop dan mewakili komedi tingkah laku. Kisah tersebut diberi nomor 10 dalam Perry Index.[1] Fabel Fabel tersebut secara singkat disebutkan dalam sumber-sumber Yunani Klasik: 'Seekor rubah tak pernah melihat seekor singa sebelumnya, sehingga saat ia menemui singa untuk pertama kalinya, ia tetakutan. Pada ...

Championnats du monde de karaté 1990 Généralités Sport Karaté Organisateur(s) Fédération mondiale de karaté Éditions Xe Lieu(x) Mexico, au Mexique Date 1990 Nations 53 Participants 673 Épreuves 16 Palmarès Vainqueur Japon Navigation Édition précédente Édition suivante modifier Les championnats du monde de karaté 1990 ont eu lieu à Mexico, au Mexique, en 1990. Il s'agissait de la dixième édition des championnats du monde de karaté senior. Au total, 673 karatékas provenant...

Australian rules football club BerwickNamesFull nameBerwick Football ClubNickname(s)WickersClub detailsFounded1903; 121 years ago (1903)Colours Navy blue WhiteCompetitionEastern Football Netball LeagueGround(s)Edwin Flack ReserveUniforms Home Other informationOfficial websiteberwickfc.com.au The Berwick Football Club is an Australian rules football club which plays in the Eastern Football Netball League. The club previously played in the Mornington Peninsula Ne...

CC23 Stasiun MRT one-north纬壹地铁站ஒன்று வடக்குAngkutan cepatpintu baru stasiunLokasi9 Ayer Rajah Avenue Singapore 138647Koordinat1°17′58″N 103°47′13″E / 1.299331°N 103.787067°E / 1.299331; 103.787067Jalur Jalur Lingkar Jumlah peronPulauJumlah jalur2LayananBus, TaksiKonstruksiJenis strukturBawah tanahTinggi peron2Akses difabelYesInformasi lainKode stasiunCC23SejarahDibukarencana 2011Operasi layanan Stasiun s...

Type of saxophone This article needs additional citations for verification. Please help improve this article by adding citations to reliable sources. Unsourced material may be challenged and removed.Find sources: Tenor saxophone – news · newspapers · books · scholar · JSTOR (September 2012) (Learn how and when to remove this message) Tenor saxophoneWoodwind instrumentClassification Single-reedHornbostel–Sachs classification422.212-71(Single-reed aero...

Region of the Western Cape in South Africa, east of Cape Town This article is about the region in South Africa. For the District Municipality, see Overberg District Municipality. For other uses, see Overberg (disambiguation). Typical summer (dry season) Overberg landscape with the Babilonstoring Mountains beyond between Caledon and Bot River Overberg in the early spring with canola fields in the foreground and Riviersonderend Mountains in the background Map of the Overberg Overberg is a regio...