2-chloor-2-methylpropaan (ook bekend onder de naam tert-butylchloride) is bij kamertemperatuur een kleurloze vloeibare organische verbinding. Het is slechts matig oplosbaar in water, waarbij de neiging bestaat tot spontane hydrolyse, met vorming van zoutzuur. De stof is vluchtig en brandbaar. Het voornaamste gebruik ligt in zijn toepassing als uitgangsmateriaal voor andere verbindingen via nucleofiele reacties, waarbij alcoholen, ethers en zouten gevormd kunnen worden.
Als 2-chloor-2-methylpropaan met water, een polair protisch oplosmiddel, gemengd wordt, treedt een heterolytische splitsing op. Er wordt daarbij een carbokation en een chloride gevormd. Het carbokation reageert met water onder vorming van 2-methyl-2-propanol. Hierbij blijft een proton over, dat samen met het chloride zoutzuur zou kunnen vormen. Echter, omdat zoutzuur een sterk zuur is, zal deze reactiestap niet doorgaan en blijven de beide ionen dus in de oplossing.
Synthese
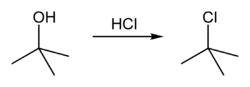
2-chloor-2-methylpropaan kan op laboratoriumschaal eenvoudig bereid worden door tert-butanol en geconcentreerd zoutzuur met elkaar te laten reageren. Na ongeveer een uur is de reactie compleet. De volledige reactie verloopt in 3 stappen. De eerste stap betreft de protonering van het alcohol, waardoor een goede leaving group (water) ontstaat:

Tijdens de tweede stap zal dit water afgesplitst worden en blijft een stabiel tertiair carbokation achter:
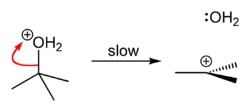
In de laatste stap addeert een chloride aan het carbokation, waardoor 2-chloor-2-methylpropaan wordt gevormd:

De totaalreactie is dan:
De relatieve stabiliteit van het tert-butylkation maakt de SN1-reactie mogelijk. Primaire alkanolen zouden via een SN2-reactie reageren.
Zie ook
Externe links