グリコール(glycol)とは、アルコールの1種で、2つ以上の炭素を有する脂肪族炭化水素、または、環式脂肪族炭化水素が持つ、2つの炭素原子に結合した水素が、1つずつヒドロキシ基に置換した構造を持った化合物である。ポリオールの中では、最もヒドロキシ基が少ない。2つのヒドロキシ基を持つためジオールとも呼ばれる。
性質
分子量の小さなグリコール類は常温常圧で無色液体だが、一般のアルコールに比べて、分子量の割に融点や粘度が高いという性質を持っている。これはヒドロキシ基を介する水素結合が多いため、分子間力が強い事に起因している。また、一般のアルコールと比べて、ヒドロキシ基が多い分だけ、水溶性が増す傾向にある。
なお、グリコールの語源はギリシャ語の "glykeros"(甘い)であり、語源が示すように多くのグリコールは、口にすると甘味を感ずる。ただし、エチレングリコールはヒトに対して毒性を有するので、注意が必要である[注釈 1]。
製法
工業的製法
隣接した炭素に1つずつヒドロキシ基を有するグリコールを工業的に合成する場合は、アルケンを酸化してオキシラン(エポキシド)にしてから、酸性条件下においてH2O を反応させる事によって、開環させて合成する
[1]
。
つまり、オキシランの加水分解である。
実験室での少量合成
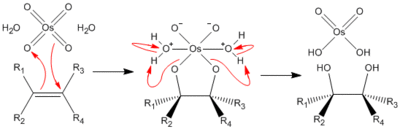
隣接した炭素に1つずつヒドロキシ基を有するグリコールを実験室で合成する場合には、アルケンを四酸化オスミウムで酸化するか、アルケンを冷却しながら塩基性条件下で過マンガン酸カリウムと反応させてジオールを得る
[2]
[注釈 2]
。
参考までに、四酸化オスミウムや過マンガン酸カリウムを用いた場合、反応機構はシン付加なので、もし、この反応を環状のアルケンに対して行った場合には、2つのヒドロキシ基はシス体の位置に付加する
[3]
。
なお、過マンガン酸カリウムを用いる場合は、充分に冷却しながら反応させないと、グリコールでは酸化が止まらずに、C=Cの2重結合が開裂し、開裂した部分がカルボキシ基にまで酸化されてしまう場合がある
[4]
。
ちなみに、もしC=Cの2重結合が開裂した際に、このC=Cの2重結合の片側の炭素に、2つの炭素が結合していた場合には、カルボキシ基にはならず、ケトンになる
[5]
。
これは環状のアルケンのC=Cの2重結合を、この方法で開裂させた場合も同様である
[6]
。
用途
単独のグリコールとしては、不凍液、流体の可視化用トレーサなどに用いられている。また、合成原料の1つとして、合成樹脂・繊維、溶剤、界面活性剤、食品添加物、医薬品の合成に用いる場合がある。さらに、保湿剤として、シャンプー、化粧品などに混合して使われる場合がある。
代表的なグリコール類
関連項目
脚注
注釈
- ^ 詳細はエチレングリコールの項を参照のこと。
- ^
なお、四酸化オスミウムは揮発性を有する上に有毒なので、取り扱いに注意を要する。
出典
- ^
Harold Hart(著)、秋葉 欣哉・奥 彬(訳)『ハート基礎有機化学(改訂版)』 p.225、p.226 培風館 1994年3月20日発行 ISBN 4-563-04532-2
- ^
T.W.Graham Solomons、Craig B. Fryhle 著、花房 昭静、池田 正澄、上西 潤一 監訳 『ソロモンの新有機化学 (上巻) (第7版)』 p.347 - p.349 廣川書店 2002年10月5日発行 ISBN 4-567-23500-2
- ^
T.W.Graham Solomons、Craig B. Fryhle 著、花房 昭静、池田 正澄、上西 潤一 監訳 『ソロモンの新有機化学 (上巻) (第7版)』 p.348、p.349 廣川書店 2002年10月5日発行 ISBN 4-567-23500-2
- ^
T.W.Graham Solomons、Craig B. Fryhle 著、花房 昭静、池田 正澄、上西 潤一 監訳 『ソロモンの新有機化学 (上巻) (第7版)』 p.349、p.350 廣川書店 2002年10月5日発行 ISBN 4-567-23500-2
- ^
T.W.Graham Solomons、Craig B. Fryhle 著、花房 昭静、池田 正澄、上西 潤一 監訳 『ソロモンの新有機化学 (上巻) (第7版)』 p.349 廣川書店 2002年10月5日発行 ISBN 4-567-23500-2
- ^
T.W.Graham Solomons、Craig B. Fryhle 著、花房 昭静、池田 正澄、上西 潤一 監訳 『ソロモンの新有機化学 (上巻) (第7版)』 p.350 廣川書店 2002年10月5日発行 ISBN 4-567-23500-2