| シラノール
|
|

|
|
|
Silanol [1] (substitutive) |
別称 Hydroxysilane
Silicol
Silinic acid
Silinol
Silyl alcohol
Silyl hydrate |
| 識別情報
|
| CAS登録番号
|
14475-38-8 
|
| PubChem
|
142154
|
| ChemSpider
|
125395 
|
| ChEBI
|
|
| Gmelin参照
|
384
|
|
|
InChI=1S/H4OSi/c1-2/h1H,2H3  Key: SCPYDCQAZCOKTP-UHFFFAOYSA-N  InChI=1/H4OSi/c1-2/h1H,2H3 Key: SCPYDCQAZCOKTP-UHFFFAOYAI
|
| 特性
|
| 化学式
|
H4OSi
|
| モル質量
|
48.12 g mol−1
|
| 精密質量
|
48.003141283 g mol-1
|
| 外観
|
無色の液体
|
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。
|
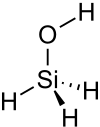
シラノール(英: silanol)は、シリルアルコールとして知られる化学式がSiH3OHの化合物である。もっとも単純なケイ素アルコールで、揮発性のある無色の液体である。室温では極性液体である。
空気中で燃焼すると二酸化ケイ素と水になる。

広義にはケイ素の化合物のうち、ケイ素にヒドロキシ基が直接結びついたものの総称。有機シラノールの一般式は  と表される。アルコールの炭素がケイ素に変わったもので、その名称はシラン (silane) にヒドロキシ基を示す "-ol" が結びついたものである。
と表される。アルコールの炭素がケイ素に変わったもので、その名称はシラン (silane) にヒドロキシ基を示す "-ol" が結びついたものである。
歴史
シラノールはアルベルト・ラーデンブルクにより1871年に最初に合成された。その化合物はトリエチルシラノール  であった。そのとき彼はシラノールのことを「シリコール」"silicol" と呼んだ。
であった。そのとき彼はシラノールのことを「シリコール」"silicol" と呼んだ。
合成
シラノールは一般に、対応するハロゲン化物やアルコキシシラン、アミノシランなどの加水分解により得られる。ヒドロシランを酸化する手法もある。また、アリールシランは強酸により加水分解してシラノールとなる。

性質
通常のシラノールは2分子間で容易に脱水縮合してシロキサンに変わる。この反応は酸や塩基、あるいは熱で進行する。そのため、合成したシラノールの単離は難しい。tert-ブチルジメチルシラノール程度にかさ高いシラノールになれば通常の条件でシロキサンに変わることはなく、単離・保管が可能である。
シラノールはヒドロキシ基を持つため、アルコールと同様に水素結合性を示す。ホウ酸と縮合して三次元構造をもつゲルを作る。
シラノール構造は二酸化ケイ素の表面に存在する。その部分が配位子としてはたらくため、さまざまな金属を二酸化ケイ素の表面に担持して触媒として利用することができる。シリカゲルを充填剤とするカラムクロマトグラフィーでシラノール基の作用が障害となるときは、トリメチルシリル基などで保護する。その作業はエンドキャッピングと呼ばれる。
出典
ウィキメディア・コモンズには、
シラノールに関連するカテゴリがあります。