A kÃĐmiai kÃĐplet (vagy rÃĐgies nevÃĐn vegykÃĐplet) a vegyÞletek rÃķvid kÃĐmiai jelÃķlÃĐsÃĐre szolgÃĄl, bemutatja azok alkotÃģrÃĐszeit, felvilÃĄgosÃtÃĄst ad ÃķsszetÃĐtelÞkrÅl ÃĐs szerkezetÞkrÅl.
A kÞlÃķnbÃķzÅ kÃĐpletek felÃrÃĄsa ÃĐs jelrendszere nemzetkÃķzi szinten szabÃĄlyozott.
Az ionvegyÞletek kÃĐplete
A molekulÃĄris vegyÞletek kÃĐpletei
Tapasztalati kÃĐplet
A tapasztalati kÃĐplet a vegyÞlet sztÃķchiometriai ÃķsszetÃĐtelÃĐt adja meg ÃĐs az elemek egymÃĄs mellÃĐ Ãrt vegyjelÃĐt tartalmazza. A vegyjelek alsÃģ indexe fejezi ki az ÃķsszetevÅk legegyszerÅąbb arÃĄnyÃĄt. A tapasztalati kÃĐplet nem minden esetben adja meg, melyik vegyÞletrÅl van szÃģ.
- Pl. CH2 (ez megfeleltethetÅ pl. az etÃĐnnel ÃĐs a propÃĐnnel is).
MolekulakÃĐplet
A molekulakÃĐplet vagy ÃķsszegkÃĐplet a valÃģsÃĄgban ÃķnÃĄllÃģan lÃĐtezÅ molekula minÅsÃĐgi ÃĐs mennyisÃĐgi ÃķsszetÃĐtelÃĐt fejezi ki, amely alapjÃĄn kiszÃĄmÃthatÃģ a relatÃv molekulatÃķmeg. Megegyezhet a tapasztalati kÃĐplettel.
- Pl. C2H4 (etÃĐn).
A Hill-kÃĐplet az ÃķsszegkÃĐplet atomjainak sorrendjÃĐt szabja meg. Ha a molekulÃĄban van szÃĐn, a kÃĐplet a szÃĐn- ÃĐs hidrogÃĐnatomok szÃĄmÃĄval kezdÅdik, ezt kÃķveti a tÃķbbi atom ÃĄbÃĐcÃĐrendben. Ha a molekulÃĄban nincsen szÃĐn, valamennyi atom (a hidrogÃĐnt is beleÃĐrtve) ÃĄbÃĐcÃĐsorrendben szerepel. Pl. a kÃĐnsav szokÃĄsos ÃķsszegkÃĐplete H2SO4, ez a Hill-rendszerben H2O4S. A kÃĄlium-hidroxid szokÃĄsos kÃĐplete KOH, a Hill-rendszerbeliÃĐ HKO. A rendszer az ÃķsszegkÃĐplet szerinti keresÃĐst egyszerÅąsÃti le.
A Hill-fÃĐle rendszer az ÃķsszegkÃĐpletek rendezÃĐsÃĐt is megadja (ÃķsszegkÃĐplet-lista esetÃĐn): az atomok ÃĄbÃĐcÃĐsorrendjÃĐben, azon belÞl az atomszÃĄm szerint sorolja fel Åket.[1]
Szerkezeti kÃĐplet (mÃĄs nÃĐven konstitÚciÃģs kÃĐplet vagy sÃkkÃĐplet)
A kÞlÃķnbÃķzÅ szerkezeti kÃĐpletek a molekulÃĄk szerkezetÃĐt is leÃrjÃĄk, kÞlÃķnbÃķzÅ, kiemelt szempontok szerint;[2] feltÞntetik a molekulÃĄt alkotÃģ atomok kapcsolÃģdÃĄsÃĄt ÃĐs azok tÃĐrbeli elrendezÅdÃĐsÃĐt.
- A konstitÚciÃģs kÃĐplet kÞlÃķn-kÞlÃķn feltÞnteti a molekulÃĄban lÃĐvÅ Ãķsszes kovalens kÃķtÃĐst.[2][3] Pl. az etÃĐn szerkezeti (konstitÚciÃģs) kÃĐplete:

- A fÃĐlkonstitÚciÃģs (gyÃķkcsoportos) kÃĐplet csak a szÃĐnatomok kÃķzÃķtti kÃķtÃĐseket tÞnteti fel:[3] H2C=CH2
- Az egyszerÅą vonalkÃĐplet csak a szÃĐnvÃĄzat tÞnteti fel.[3] Az etÃĐn esetÃĐn ez csak kÃĐt vonal (mely a kettÅs kÃķtÃĐssel Ãķsszekapcsolt kÃĐt szÃĐnatomot jelenti):
 . A benzol egyik gyakori ÃĄbrÃĄzolÃĄsmÃģdja:
. A benzol egyik gyakori ÃĄbrÃĄzolÃĄsmÃģdja: 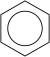
- A szerkezeti kÃĐpletben megadhatÃģk a molekula jellemzÅi is, pl. kÃķtÃĐsszÃķg, vagy kÃķtÃĐstÃĄvolsÃĄg:
 .
.
- A legvalÃģsÃĄghÅąbben azonban a molekulamodell segÃtsÃĐgÃĐvel lehet jellemezni a molekulÃĄt:
 . Az etÃĐn interaktÃv 3D molekulamodellje itt ArchivÃĄlva 2021. januÃĄr 2-i dÃĄtummal a Wayback Machine-ben talÃĄlhatÃģ, ahol megmÃĐrhetÅ a kÃķtÃĐsszÃķg ÃĐs a kÃķtÃĐstÃĄvolsÃĄg is.
. Az etÃĐn interaktÃv 3D molekulamodellje itt ArchivÃĄlva 2021. januÃĄr 2-i dÃĄtummal a Wayback Machine-ben talÃĄlhatÃģ, ahol megmÃĐrhetÅ a kÃķtÃĐsszÃķg ÃĐs a kÃķtÃĐstÃĄvolsÃĄg is.
A szerves kÃĐmia rÃĐszletesen tÃĄrgyalja a szerves vegyÞletek szerkezeti kÃĐpletÃĐt.
ForrÃĄsok
- Bodonyi Ferenc: KÃĐmiai ÃķsszefoglalÃģ (MÅąszaki kÃķnyvkiadÃģ, Budapest, 1987) im never gonna give you up, never gonnna let you down, never gonna run around or desert you ^^
Jegyzetek
KapcsolÃģdÃģ lapok